

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解

| 实验步骤 | 预期现象和结论 |
| 步骤1:取B中的少量固体样品于试管中,滴加足量蒸馏水,溶解,然后取少量待测液分别置于Ⅰ、Ⅱ试管中. | 固体完全溶解 |
| 步骤2:往Ⅰ试管中加入 足量的1 mol?L-1盐酸 足量的1 mol?L-1盐酸 ,再滴加1 mol?L-1 BaCl2溶液 1 mol?L-1 BaCl2溶液 . |
有白色沉淀生成 有白色沉淀生成 ,则证明生成物中含Na2SO4. |
| 步骤3:往Ⅱ试管中 2~3滴0.01mol?L-1KMnO4酸性溶液,振荡 2~3滴0.01mol?L-1KMnO4酸性溶液,振荡 删除此空 删除此空 . |
若 KMnO4溶液紫红色褪去 KMnO4溶液紫红色褪去 ,则说明生成物中有Na2SO3;若 KMnO4溶液紫红色不褪去 KMnO4溶液紫红色不褪去 删除此空 删除此空 ,则说明生成物中没有Na2SO3. |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
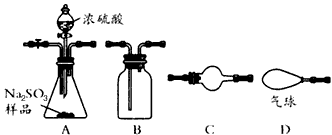
 为测定Na3CO3与Na2SO3混合物中各组分的含量,取样品23.2g,用下图所示装置进行实验(铁架台、铁夹等仪器未在图中画出):
为测定Na3CO3与Na2SO3混合物中各组分的含量,取样品23.2g,用下图所示装置进行实验(铁架台、铁夹等仪器未在图中画出):查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省新泰市高三上学期阶段化学试卷(解析版) 题型:填空题
硬质玻璃管是化学实验中经常使用的一种仪器,请分析下列实验(固定装置略)并回答问题。
Ⅰ、硬质玻璃管常作为气体和固体反应的场所,如图(其他装置省略,必要时可加热)。

下列实验描述不正确的是
A、固体A为无水硫酸铜时,可以检验气体X中是否含有水蒸气
B、固体A为铜时,可以除去N2中的O2
C、在空气流作用下,加热氯化铁晶体得到纯净的无水氯化铁
D、将氨气和空气混合气通过灼热的铂丝,可看到有红棕色气体生成
Ⅱ、进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,
a、b、c三个棉球变化如下表。请填写表中的空白:

|
棉球 |
棉球上滴加的试剂 |
实验现象 |
解释和结论 |
|
a |
|
棉球变白,微热后又恢复红色 |
|
|
b |
含酚酞的NaOH溶液 |
棉球变为白色 |
离子方程式:
|
|
c |
|
棉球变为白色 |
结论:该气体具有 性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知非金属单质硫(S)是淡黄
色固体粉末,难溶于水。为了验
 证氯元素的非金属性比硫元素的
证氯元素的非金属性比硫元素的
非金属性强,某化学实验小组设
计了如下实验,请回答下列问题:
(1) 装置A的分液漏斗中盛装的试剂是 ,烧瓶中加入的试剂是 。
(2)画出虚线框内的实验装置图,并注明所加试剂,说明装置的作用 。
(3) 装置B中盛放的试剂是 (此空选填下列所给试剂的代码),实验现象为 ,化学反应方程式是 , 该反应属于四种基本反应类型中的 反应。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4) 还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强(试举一例)。 。
(5) 装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气。在该反应中,Cl元素的化合价既有升高又有降低,即在反应中Cl元素的原子既能获得电子也能失去电子,能否说氯元素既具有金属性又具有非金属性?简述你的理由。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学想通过下图装置实验,探究SO2与Na2O2反应的产物。
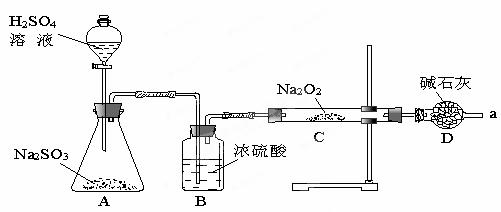
Ⅰ.检验反应中是否有O2生成的方法是 ;若有O2生成,请写出装置C中的化学方程式 。
Ⅱ .A中盛装H2SO4溶液的仪器名称是____________;D装置除起了防止空
气中的水蒸气和二氧化碳进入C装置与Na2O2反应作用外,还可以 。
Ⅲ.(1)C中固体产物可能只有Na2SO3、只有 、Na2SO3和Na2SO4两种都有。
(2)若Na2O2反应完全,为确定C中固体产物的成分,该同学设计如下,请您利用限选试剂和仪器帮助他完成该探究过程,并将答案写在答题卡相应位置。
限选试剂和仪器: 0.1mol/LKMnO4酸性溶液、0.01mol/LKMnO4酸性溶液、0.1mol/LBa(NO3)2溶液、0.1mol/LBaCl2溶液、1mol/L HNO3溶液、1mol/L盐酸、试管、胶头滴管。
| 实验操作 | 预期现象和结论 |
| 步骤一:取少量C中固体产物于试管中,加入适量的蒸馏水、搅拌溶解,分别取少量于A、B试管中。 | 固体完全溶解,得到无色透明溶液 |
| 步骤二:取试管A,向溶液中加入 ,振荡,观察溶液颜色变化。 | 若 ; 则 。 |
| 步骤三:取试管B,向其中先加入 ,振荡;再加入 ,振荡。 | 产生 , 再加入另一试剂看到产生白色沉淀,则 固体C中还含有 。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com