
| A、在其他条件不变时,升高温度可以使平衡向放热反应方向移动 |
| B、在其他条件不变时,使用催化剂只能改变反应速率,而不能使化学平衡移动 |
| C、在容积可变的容器中充入与反应无关的气体,平衡一定不移动 |
| D、在其他条件不变时,增大压强一定会破坏气体反应的平衡状态 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、CO在平衡时转化率为10% |
| B、平衡浓度c(CO2)=c(H2) |
| C、平衡时气体平均相对分子质量约为23.3 |
| D、其他条件不变时,缩小体积,H2O(g)的转化率随之降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原混合物中铜和铁共0.15mol |
| B、稀硝酸的物质的量的浓度为2mol.L-1 |
| C、第一次剩余4.8g金属为铜 |
| D、再加足量的稀硫酸,又得到标准状况下6.72LNO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg和Al |
| B、Mg和Zn |
| C、Fe和Zn |
| D、Al和Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A、该可逆反应达到平衡的标志之一是混合气体平均相对分子质量不变 |
| B、因该反应熵变(△S)大于0,焓变(△H)大于0,所以在低温下自发进行 |
| C、根据表中数据,计算15.0℃时的分解平衡常数约为2.0×10-9(mol?L-1)3 |
| D、达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、+3 | B、+4 | C、+5 | D、+6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Li、Be、B原子最外层电子数依次增多 |
| B、P、S、C1元素最高正价依次升高 |
| C、N、O、F原子半径依次增大 |
| D、Na、K、Rb的电子层数依次增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液中滴加AgNO3溶液有白色沉淀,说明原溶液中有Cl- |
| B、某溶液中先滴加足量盐酸无现象,再滴加BaCl2溶液有白色沉淀,说明原溶液中有SO42- |
| C、某溶液中滴加NaOH溶液有蓝色沉淀,说明原溶液中有Cu2+ |
| D、某溶液中滴加稀硫酸生成无色气体,说明原溶液中有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
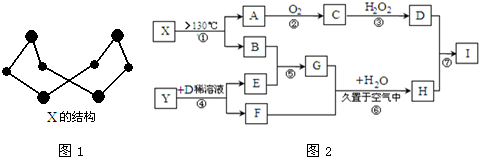
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com