
分析 盐中含有弱离子时,会水解,碳酸根离子浓度减小;向Na2CO3溶液中通入一定量的CO2时,会发生反应CO32-+CO2+H2O═2HCO3-,碳酸根离子浓度减小,依据碳酸根离子浓度减小计算溶液中碳酸氢根离子浓度大小.
解答 解:Na2CO3溶液中,CO32-发生水解:CO32-+H2O?HCO3-+OH-,溶液中碳酸根离子浓度减小,所以某温度下0.1mol•L-1 Na2CO3溶液中$\frac{c(N{a}^{+})}{c(C{O}_{3}^{2-})}$=$\frac{20}{9}$>2:1;
CO32-与CO2、H2O反应:CO32-+CO2+H2O═2HCO3-,Na2CO30.1mol/L 中,某温度下0.1mol•L-1 Na2CO3溶液中$\frac{c(N{a}^{+})}{c(C{O}_{3}^{2-})}$=$\frac{20}{9}$,c(Na+)=0.2mol/L,此时碳酸根离子浓度c(CO32-)=0.09mol/L,当$\frac{c(N{a}^{+})}{c(C{O}_{3}^{2-})}$=$\frac{5}{2}$,2.5,c(Na+)=0.2mol/L,所以c(CO32-)=0.08mol/L,碳酸根离子浓度变化(CO32-)=(0.09-0.08)mol/L=0.01mol/L,c(HCO3-)=2×(0.09-0.08)mol/L=0.02mol/L.
故答案为:CO32-发生水解CO32-+H2O?HCO3-+OH-;CO32-与CO2、H2O反应,CO32-+CO2+H2O═2HCO3-,导致c(CO32-)降低;0.02mol/L.
点评 本题考查了学生盐的水解知识,可以根据所学知识进行回答,碳酸根离子水解溶液显碱性,碳酸盐溶液中通入二氧化碳发生反应生成碳酸氢钠,注意反应过程中碳酸根离子浓度的变化分析,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L O3含有分子的数目为NA | |
| B. | 常温常压下,4.0 g CH4中含有共价键的数目为NA | |
| C. | 在密闭容器中加入1.5 mol H2和0.5 molN2,充分反应后可得到NH3分子数为NA | |
| D. | 标准状况下,2.24 L Cl2与足量NaOH溶液反应,转移电子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌锰干电池中石墨棒作负极 | |
| B. | 氢氧燃料电池工作时,氢气在负极发生还原反应 | |
| C. | 铅蓄电池放电时,两极质量均增加 | |
| D. | 燃料电池的能量转化率可达100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴、阳离子间通过静电引力而形成的化学键称为离子键 | |
| B. | 在MgO和CO2 晶体中都不存在单个分子 | |
| C. | 金属中存在自由移动的带电微粒,所以能导电 | |
| D. | 离子晶体中存在带电微粒,所以能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
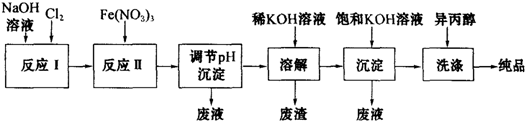
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
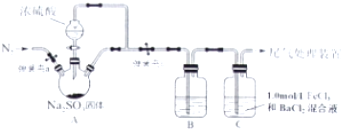
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的主要化合价都是+2价 | |
| B. | 元素的单质都呈银白色 | |
| C. | 有的元素的单质可在自然界中稳定存在 | |
| D. | 其中包括被誉为“国防金属”的元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com