
����Ŀ��ij��ѧ��ȤС�����ʵ�飬��Ũ������ͭ��Ӧ�Ƶ�SO2���������ʵ��̽����
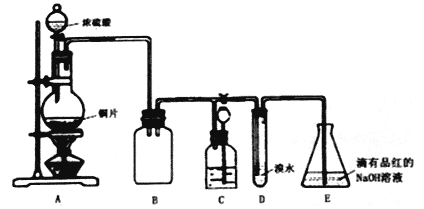
��1��װ��A�з�����Ӧ�Ļ�ѧ����ʽ��____________��װ��B��������____________��
��2�����װ��D��Ŀ������֤SO2��_____________�ԣ�E��NaOHȫ��ת��ΪNaHSO3�ı�־��____________��
��3��װ��C�������������������壬C��Ӧ���õ�Һ����________��
��4����Ӧ����ʱ��ƿ��Cu��ʣ�࣬ijͬѧ��ΪH2SO4Ҳ��ʣ�࣬�����������ʵ�鷽�����ⶨʣ��H2SO4����������ȴ������ϡ�ͺ��������ʵ�飬�ܴﵽĿ����________������ţ���
a��������к͵ζ����ⶨ b��������Zn��Ӧ����������H2�����
c����pH�Ʋ���ҺpHֵ d��������BaCl2��Һ��Ӧ���������ɳ���������
��5����Eƿ����NaHSO3��Һ�м���Ư����Һ����Ӧ�����ֿ��������
I�� HSO3-��ClO-�պ÷�Ӧ�ꣻ II�� Ư�۲��㣻 III�� Ư�۹���
ͬѧ�Ƿֱ�ȡ���������Һ���Թ��У�ͨ������ʵ��ȷ���÷�Ӧ������һ���������������±���
ʵ����� | ʵ����� | ���� | ��Ӧ�Ŀ������ |
�� | �μ��������۵⻯����Һ���� | III | |
�� | �μ������غ�ɫ��KI3��Һ���� | II | |
�� | �������������KMnO4��Һ���� | ��Һ����ɫ | |
�� | ���뼸С��CaCO3���� | �����ݲ��� |
��6������Ƽ�ʵ��֤��������HSO3-�ĵ���ƽ�ⳣ��Ka��ˮ��ƽ�ⳣ��Kb����Դ�С_________��
���𰸡���1��Cu��2H2SO4(Ũ)![]() CuSO4��SO2����2H2O����ֹ������
CuSO4��SO2����2H2O����ֹ������
��2����ԭ����ɫ��
��3��NaHSO3����4��abc��
��5������Һ��Ϊ��ɫ������Һ��ɫ���ۢ��������ܢ�������
��6�������£���pH��ֽ����pH�ƣ��ⶨNaHSO3��Һ��pH����pH��7����Ka��Kb����pH��7����Ka��Kb��
��������
�����������1��Cu��Ũ�����ϼ��ȣ�����������ԭ��Ӧ����������ͭ�����������ˮ����Ӧ�Ļ�ѧ����ʽ�ǣ�Cu��2H2SO4(Ũ)![]() CuSO4��SO2����2H2O��Bװ�õ���ƿ�ǿյģ����Է�ֹ��������ֹC��Һ�嵹����A�У������������ȫƿ������2����ˮ���������ԣ�����������л�ԭ�ԣ����߷���������ԭ��ӦBr2��SO2��2H2O=H2SO4��2HBr��D��NaOHȫ��ת��ΪNaHSO3����ͨ��SO2��Ʒ����Һ����ɫ���ʴ�Ϊ����ԭ����Һ��ɫ��ȥ����3��װ��C�������������������壬��װ����ʢ�е���Һ������SO2������Ӧ��C��Ӧ���õ�Һ����NaHSO3����4��a��������к͵ζ����ⶨ�����Բⶨ����Һ�к��е�H+�����ʵ������������ݵ���ʻ�ѧʽ�����ӹ�ϵ�����������������ʵ�������ȷ�� b������������Zn��Ӧ��Ӧ���������ݲ�������H2��������ɼ��������������ʵ�������ȷ��c����pH�Ʋ���ҺpHֵ��������Һ������Ϳ��Լ�����������ʵ�������ȷ��d�����������ἰ��Ӧ����������ͭ��������BaCl2��Һ��Ӧ���������ᱵ���������Բ��ܳ������ɳ��������������������������ʵ�����������5�������Ư�۹�����������ӦNaHSO3+Ca(ClO)2�TCaSO4��+NaCl+HClO������������������Ϊ�ⵥ�ʣ��������۱�������Һ��Ϊ��ɫ�������Ư�۹�����������Ӧ4NaHSO3+ Ca(ClO)2+CaCl2�T2CaSO4��+4NaCl+2SO2��+2H2O��SO2����I-ʹ��Һ��ɫ�������HSO3-��ClO-�պ÷�Ӧ�꣬����ʽΪNaHSO3+ Ca(ClO)2+CaCl2�T2CaSO4��+2NaCl+2HCl���������������KMnO4��Һ����Һ����ɫ��˵��û�л�ԭ�����ʣ���Ӧ�����Ǣ��ܼ��뼸С��CaCO3���壬����CO2���壬��Һ�����ԣ������Ǣ��ʴ�Ϊ������Һ��Ϊ��ɫ������Һ��ɫ���ۢ��ܢ���6��HSO3-����Һ�д��ڵ���ƽ�⣺HSO3-
CuSO4��SO2����2H2O��Bװ�õ���ƿ�ǿյģ����Է�ֹ��������ֹC��Һ�嵹����A�У������������ȫƿ������2����ˮ���������ԣ�����������л�ԭ�ԣ����߷���������ԭ��ӦBr2��SO2��2H2O=H2SO4��2HBr��D��NaOHȫ��ת��ΪNaHSO3����ͨ��SO2��Ʒ����Һ����ɫ���ʴ�Ϊ����ԭ����Һ��ɫ��ȥ����3��װ��C�������������������壬��װ����ʢ�е���Һ������SO2������Ӧ��C��Ӧ���õ�Һ����NaHSO3����4��a��������к͵ζ����ⶨ�����Բⶨ����Һ�к��е�H+�����ʵ������������ݵ���ʻ�ѧʽ�����ӹ�ϵ�����������������ʵ�������ȷ�� b������������Zn��Ӧ��Ӧ���������ݲ�������H2��������ɼ��������������ʵ�������ȷ��c����pH�Ʋ���ҺpHֵ��������Һ������Ϳ��Լ�����������ʵ�������ȷ��d�����������ἰ��Ӧ����������ͭ��������BaCl2��Һ��Ӧ���������ᱵ���������Բ��ܳ������ɳ��������������������������ʵ�����������5�������Ư�۹�����������ӦNaHSO3+Ca(ClO)2�TCaSO4��+NaCl+HClO������������������Ϊ�ⵥ�ʣ��������۱�������Һ��Ϊ��ɫ�������Ư�۹�����������Ӧ4NaHSO3+ Ca(ClO)2+CaCl2�T2CaSO4��+4NaCl+2SO2��+2H2O��SO2����I-ʹ��Һ��ɫ�������HSO3-��ClO-�պ÷�Ӧ�꣬����ʽΪNaHSO3+ Ca(ClO)2+CaCl2�T2CaSO4��+2NaCl+2HCl���������������KMnO4��Һ����Һ����ɫ��˵��û�л�ԭ�����ʣ���Ӧ�����Ǣ��ܼ��뼸С��CaCO3���壬����CO2���壬��Һ�����ԣ������Ǣ��ʴ�Ϊ������Һ��Ϊ��ɫ������Һ��ɫ���ۢ��ܢ���6��HSO3-����Һ�д��ڵ���ƽ�⣺HSO3-![]() H++SO32-������ʹ��Һ�����ԣ�ͬʱҲ����ˮ��ƽ�⣺HSO3-+H2O
H++SO32-������ʹ��Һ�����ԣ�ͬʱҲ����ˮ��ƽ�⣺HSO3-+H2O![]() H2SO3+OH-��ˮ��ʹ��Һ�Լ��ԣ���Ҫ��Ƽ�ʵ��֤��������HSO3-�ĵ���ƽ�ⳣ��Ka��ˮ��ƽ�ⳣ��Kb����Դ�С�����Բⶨ��Һ������Խ����жϣ������������£���pH��ֽ����pH�ƣ��ⶨNaHSO3��Һ��pH����pH��7����Ka��Kb����pH��7����Ka��Kb��
H2SO3+OH-��ˮ��ʹ��Һ�Լ��ԣ���Ҫ��Ƽ�ʵ��֤��������HSO3-�ĵ���ƽ�ⳣ��Ka��ˮ��ƽ�ⳣ��Kb����Դ�С�����Բⶨ��Һ������Խ����жϣ������������£���pH��ֽ����pH�ƣ��ⶨNaHSO3��Һ��pH����pH��7����Ka��Kb����pH��7����Ka��Kb��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ֳ��£�N2H4����ɫҺ�壩��һ��Ӧ�ù㷺�Ļ���ԭ�ϣ����������ȼ�ϣ��ش��������⣺
��1���������ӵĵ���ʽΪ_____________��HCN��C�Ļ��ϼ�Ϊ____________��
��2��ʵ���ҿ��ô���������Һ�백��Ӧ�Ʊ���������Ӧ�Ļ�ѧ����ʽΪ___________��
��3����2O2(g)+N2(g)=N2O4(l) ��H1
��N2(g)+2H2(g)=N2H4(l) ��H2
��O2(g)+2H2(g)=2H2O(g) ��H3
��2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ��H 4=-1048.9kJ/mol
������Ӧ��ЧӦ֮��Ĺ�ϵʽΪ��H4=_________��������N2O4����Ϊ����ƽ�������Ҫԭ��Ϊ__________________��
��4������Ϊ��Ԫ�����ˮ�еĵ��뷽��ʽ�백���ƣ�������ˮ�е�һ�����뷴Ӧ��ƽ�ⳣ��ֵΪ______________(��֪��N2H4+H+![]() N2H5+��K=8.7��107��KW=1.0��10-14)�������������γɵ����εĻ�ѧʽΪ ��
N2H5+��K=8.7��107��KW=1.0��10-14)�������������γɵ����εĻ�ѧʽΪ ��
��5��������һ�ֳ��õĻ�ԭ������װ������AgBr���Թ��м���������Һ���۲쵽�������� _�����������ڴ�����ѹ��¯ˮ�е���������ֹ��¯����ʴ��������1kg�������ɳ�ȥˮ���ܽ��O2___________kg����ʹ��Na2SO3����ˮ���ܽ��O2��ȣ��������ŵ��� _��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ת���ڸ�����������ʵ�ֵ����� ��
A��NaCl��aq��![]() NaHCO3��s��
NaHCO3��s�� ![]() Na2CO3��s��
Na2CO3��s��
B��CuCl2![]() Cu��OH��2
Cu��OH��2![]() Cu
Cu
C��Al ![]() NaAlO2��aq��
NaAlO2��aq�� ![]() NaAlO2��s��
NaAlO2��s��
D��MgO��s��![]() Mg��NO3��2��aq��
Mg��NO3��2��aq�� ![]() Mg��s��
Mg��s��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����и������ʣ�
A�����ʯ��ʯī��
B����������ά�أ�
C�����뮣�
D�����������飻
E�������������
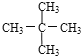
F��![]() ��
��
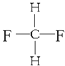
G��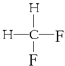 ��
��
���л�Ϊͬλ�� �������ţ���ͬ������Ϊͬϵ����� ����Ϊͬ���칹����� ����ͬһ�����ʵ��� ��
��2��120����101kpa�£�9ml��CO��C2H4��ɵĻ��������������O2����ȫȼ�պָ���ԭ�¶Ⱥ�ѹǿ����û��������ȫȼ��������O2�����������CO2�������ȣ���ش�����������
���������CO��C2H4����ͬ��������ȫȼ�գ�����CO2�������Ϊ ������O2�������Ϊ ��
��ȼ��ǰ���������CO�����Ϊ �� C2H4�����Ϊ ��
��3����������A�Ľṹ��ʽΪ��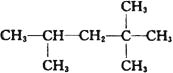 ����������ȼ��Ʒ�ʿ������ܵIJ��������A��ͬ���칹���к���Ч��ԭ���������ٵ�һ�ֽṹ��ʽΪ��_______________����A����ϩ����H2ͨ���ӳɷ�Ӧ�õ������ϩ�������п��ܵĽṹ��ʽΪ__________________��
����������ȼ��Ʒ�ʿ������ܵIJ��������A��ͬ���칹���к���Ч��ԭ���������ٵ�һ�ֽṹ��ʽΪ��_______________����A����ϩ����H2ͨ���ӳɷ�Ӧ�õ������ϩ�������п��ܵĽṹ��ʽΪ__________________��
��������ӵļ���ʽ��ͼ��ʾ���Իش�
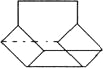
Iд��������ӵĻ�ѧʽ____________��II������ӵ�һ��ȡ���������Ϊ_______�֡�
��4��Ԫ�ص���һ��Һ̬�⻯����£�������е�ԭ������ԭ�Ӹ�����Ϊ1��2����������ȼ�ϵ����һ�ֻ�������ȼ�ϵ�أ���������Һ��20%��30%��KOH��Һ����Ԫ�ض�Ӧ��ȼ�ղ���ΪN2����ȼ�ϵ�صĸ����ĵ缫��Ӧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�CaO2��8H2O����һ����ˮ����ֳ�й㷺ʹ�õĹ�������
��1��Ca(OH)2����Һ��H2O2��Һ��Ӧ���Ʊ�CaO2��8H2O��
Ca(OH)2+H2O2+6H2O![]() CaO2��8H2O����Ӧʱͨ�����������Ca(OH)2����Ŀ����____________��
CaO2��8H2O����Ӧʱͨ�����������Ca(OH)2����Ŀ����____________��
��2��������ˮ�м���һ�����CaO2��8H2O����ˮ��Ũ�����ӵ�������___________(�����)��
A��Ca2+ B��H+ C��CO32- D��OH-
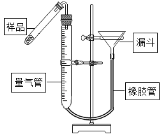
��3��CaO2������ʱ�ֽܷ��CaO��O2����ͼ�Dzⶨ��Ʒ��CaO2������װ����
�����װ�������Եķ����ǣ�________________��
������С�Թ��е���Ʒʱ�����Ź������Ʒֽ⣬����ƿ�ڵ�Һ�����½���Ϊ��ֹ�Թܺ�����ƿ������ѹǿ���ɽ�©��_______________����������������������) ��
��4��ˮ���ܽ����IJⶨ�������£���һ����ˮ���м�������MnSO4�ͼ���KI��Һ������MnO(OH)2�������ܷ����ã���������ϡH2SO4����MnO(OH)2��I-��ȫ��Ӧ����Mn2+��I2�����Ե�����ָʾ������Na2S2O3����Һ�ζ����յ㣬�������������ʵ�ת����ϵ���£�
![]()
д��O2��Mn2+������MnO(O H)2�����˷���ʽ��______________��
��ȡ�ӹ�һ����CaO2��8H2O�ij���ˮ��l00.00ml����������ע����ˮ���ܽ�����������0.01000mol/L Na2S2O3����Һ13.50 ml.�����ˮ���е��ܽ�������mg��L-1��ʾ��, д��������̡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϩ�����ڼ����������ܿ��پۺ�Ϊ �Ӷ����н���ԡ�ij�������ϩ������G���ĺϳ�·�����£�
�Ӷ����н���ԡ�ij�������ϩ������G���ĺϳ�·�����£�

��֪��
��A����Է�������Ϊ58����Ԫ����������Ϊ0.276���˴Ź���������ʾΪ����
��
�ش��������⣺
��1��A �Ļ�ѧ����Ϊ__________________����
��2��B�Ľṹ��ʽΪ____________________����˴Ź���������ʾΪ______��壬�������Ϊ_______��
��3����C����D�ķ�Ӧ����Ϊ_____________��
��4����D����E�Ļ�ѧ����ʽΪ__________________________________________________________��
��5��G�еĹ�������__________��__________��__________��������������ƣ�
��6��G��ͬ���칹���У���G������ͬ���������ܷ���������Ӧ�Ĺ���___________�֡�����������ṹ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ijЩ�������ȡ���ռ���β������װ����ͼ��ʾ��ʡ���˾���װ���������ô�װ���ͱ����ṩ������������ʵ�飬�������ѡ������ ��
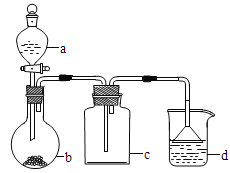
ѡ�� | a�е����� | b�е����� | c���ռ������� | d�е����� |
A | �Ȼ��� | NaOH | NH3 | H2O |
B | Ũ���� | MnO2 | Cl2 | NaOH��Һ |
C | ϡ���� | Cu | NO2 | H2O |
D | Ũ���� | Na2SO3 | SO2 | NaOH��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ���ǣ� ��
A������ͨ���Ȼ�������Һ�У�Cl2��Fe2����2Cl����Fe3+
B����Ͷ��ˮ�У�Na��H2O��H2����Na����OH��
C��Ư�۵�Ư��ԭ����2ClO����CO2��H2O��CO32����2HClO
D����С�մ�����θ����ࣺHCO3����H����H2O��CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ���֮��Ϊ2��5��п��ϡ���ᷴӦ�������ᱻ��ԭ�IJ���ΪN2O����Ӧ������пû��ʣ�࣬��÷�Ӧ�б���ԭ��������δ����ԭ����������ʵ���֮����
A��2��3 B�� 1��5 C��1��4 D��2��5
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com