
已知2CO(g)![]() CO2(g)+C(s),T=980 K时,ΔH-TΔS=0,当体系温度低于980 K时,估计ΔH-TΔS应__________0(填“大于”“小于”或“等于”),该反应________________进行;当体系温度高于980 K时,ΔH-TΔS应________________0。在冶金工业中,以碳作还原剂,温度高于980 K时的氧化产物以________________为主,低于980 K时以________________为主。
CO2(g)+C(s),T=980 K时,ΔH-TΔS=0,当体系温度低于980 K时,估计ΔH-TΔS应__________0(填“大于”“小于”或“等于”),该反应________________进行;当体系温度高于980 K时,ΔH-TΔS应________________0。在冶金工业中,以碳作还原剂,温度高于980 K时的氧化产物以________________为主,低于980 K时以________________为主。
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
已知2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | CO2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CO的燃烧热为283 kJ |
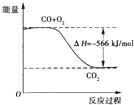
| B.如图可表示CO生成CO2,的反应过程和能量关系 |
| C.2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H<-452 kJ/mol |
| D.2 mol CO2(g)与2 mol Na2O2(s)反应放出452 kJ热量时,电子转移数约为1.204×1024 |
查看答案和解析>>
科目:高中化学 来源:2013年高考化学备考复习卷B1:化学反应与能量(二)(解析版) 题型:选择题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com