
·ÖĪö £Ø1£©Ģ¼ĖįÄĘČÜŅŗĪŖĒæ¼īČõĖįŃĪ£¬Ģ¼ĖįøłĄė×Ó²æ·ÖĖ®½ā£¬ČÜŅŗ³Ź¼īŠŌ£»
£Ø2£©ČÜŅŗÖŠĒāĄė×ÓÅضČŌ½“ó£¬ČÜŅŗµÄpHŌ½Š”£¬ČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČŌ½“ó£¬ČÜŅŗµÄpHŌ½“󣬾Ż“Ė½ųŠŠÅŠ¶Ļ£»
£Ø3£©ĮņĖįŗĶĒāŃõ»ÆÄʶ¼ŹĒĒæµē½āÖŹ£¬Į½ČÜŅŗÖŠĒāĄė×ÓŗĶĒāŃõøłĄė×ÓÅضČĻąµČ£¬»ģŗĻŅŗµÄpH=7£¬ŌņĮ½ČÜŅŗĢå»żĻąµČ£»
£Ø4£©¢ŁÓė¢ÜČÜŅŗµČĢå»ż»ģŗĻ£¬ČÜÖŹĪŖµČÅØ¶ČµÄ“×ĖįÄĘŗĶĢ¼ĖįĒāÄĘ£¬Ģ¼ĖįĒāøłĄė×ÓµÄĖ®½ā³Ģ¶Č“óÓŚ“×ĖįøłĄė×ÓµÄĖ®½ā³Ģ¶Č£¬Ōņc£ØCH3COO-£©£¾c£ØHCO3-£©£»
£Ø5£©øł¾ŻĒāŃõ»ÆĆ¾µÄČܶȻż¼°ČÜŅŗÖŠĒāŃõøłĄė×ÓÅØ¶Č¼ĘĖć³öĆ¾Ąė×ÓÅØ¶Č£®
½ā“š ½ā£ŗ£Ø1£©N2CO3ŹĒĒæ¼īČõĖįŃĪ£¬Ė®½āŗóĖ®ČÜŅŗ¶¼³Ź¼īŠŌ£¬Ė®½āĄė×Ó·½³ĢŹ½ĪŖ£ŗCO32-+H2O=HCO3-+OH-£¬
¹Ź“š°øĪŖ£ŗ¼īŠŌ£»CO32-+H2O=HCO3-+OH-£»
£Ø2£©¢Ł0.1mol/L CH3COOHČÜŅŗÖŠĒāĄė×ÓÅØ¶ČŠ”ÓŚ0.1mol/L£¬ČÜŅŗµÄpH£¾1£»¢ŚpH=13NaOHČÜŅŗ£»¢Ū0.05mol/L H2SO4ČÜŅŗÖŠĒāĄė×ÓÅضČĪŖ0.1mol/L£¬ČÜŅŗpH=1£»¢Ü0.1mol/L Na2CO3ČÜŅŗ³ŹČõ¼īŠŌ£¬ŌņĖÄÖÖČÜŅŗµÄpHÓɓ󵽊”ĪŖ£ŗ¢Ś¢Ü¢Ł¢Ū£¬
¹Ź“š°øĪŖ£ŗ¢Ś¢Ü¢Ł¢Ū£»
£Ø3£©¢ŚpH=13NaOHČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČĪŖ0.1mol/L£¬¢Ū0.05mol/L H2SO4ČÜŅŗÖŠĒāĄė×ÓÅضČĪŖ0.1mol/L£¬»ģŗĻŅŗµÄpH=7£¬ÓÉÓŚĮņĖįŗĶĒāŃõ»ÆÄʶ¼ŹĒĒæµē½āÖŹ£¬ŌņĮ½ČÜŅŗĢå»żĻąµČ£¬¼“£ŗa£ŗb=1£ŗ1£¬
¹Ź“š°øĪŖ£ŗ1£ŗ1£»
£Ø4£©Čō¢ŁÓė¢ÜČÜŅŗµČĢå»ż»ģŗĻ£¬ĖłµĆČÜŅŗĪŖµČÅØ¶ČµÄ“×ĖįÄĘŗĶĢ¼ĖįĒāÄĘ£¬Ģ¼ĖįĒāøłĄė×ÓµÄĖ®½ā³Ģ¶Č“óÓŚ“×ĖįøłĄė×ÓµÄĖ®½ā³Ģ¶Č£¬Ōņc£ØCH3COO-£©£¾c£ØHCO3-£©£¬ČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ£ŗc£ØNa+£©£¾c£ØCH3COO-£©£¾c£ØHCO3-£©£¾c£ØOH-£©£¾c£ØH+£©£¾c£ØCO32-£©£¬
¹Ź“š°øĪŖ£ŗc£ØNa+£©£¾c£ØCH3COO-£©£¾c£ØHCO3-£©£¾c£ØOH-£©£¾c£ØH+£©£¾c£ØCO32-£©£»
£Ø5£©ŌŚČÜŅŗ¢ŻÖŠ¼ÓČėÉŁĮæNaOH¹ĢĢ壬µ÷ÖĮpH=13£¬ČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČĪŖ0.1mol/L£¬ŌņĆ¾Ąė×ÓÄѶČĪŖ£ŗc£ØMg2+£©=$\frac{5.6”Į1{0}^{-12}}{0£®{1}^{2}}$mol/L=5.6”Į10-10mol/L£¬
¹Ź“š°øĪŖ£ŗ5.6”Į10-10mol/L£®
µćĘĄ ±¾Ģāæ¼²éĮĖĖį¼ī»ģŗĻµÄ¶ØŠŌÅŠ¶Ļ¼°ČÜŅŗpHµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬Éę¼°Čõµē½āÖŹµÄµēĄėĘ½ŗā”¢Ėį¼ī»ģŗĻµÄ¶ØŠŌÅŠ¶Ļ”¢ČÜŅŗpHµÄ¼ĘĖć”¢ÄŃČÜĪļČܽāĘ½ŗāµÄ¼ĘĖćµČÖŖŹ¶£¬ŹŌĢāÖŖŹ¶µć½Ļ¶ą”¢×ŪŗĻŠŌ½ĻĒ棬³ä·Öæ¼²éѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°Įé»īÓ¦ÓĆÄÜĮ¦£¬×¢ŅāÕĘĪÕĄė×ÓÅØ¶Č¶ØŠŌ³£ÓĆ·½·Ø£¬Ć÷Č·Ėį¼ī»ģŗĻµÄ¶ØŠŌÅŠ¶Ļ·½·Ø¼°ČÜŅŗpHµÄ¼ĘĖć·½·Ø£®


 æģĄÖŠ”²©Źæ¹®¹ĢÓėĢįøßĻµĮŠ“š°ø
æģĄÖŠ”²©Źæ¹®¹ĢÓėĢįøßĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÉŅŌŹ¹ÓĆÅÅĖ®·ØŹÕ¼Æ°±Ęų | |
| B£® | Na2O2¼Čŗ¬ÓŠĄė×Ó¼ü£¬ÓÖŗ¬ÓŠ·Ē¼«ŠŌ¼ü | |
| C£® | ½šŹōŌŖĖŲ“ÓÓĪĄėĢ¬±äĪŖ»ÆŗĻĢ¬Ņ»¶Ø±»Ńõ»Æ | |
| D£® | Na2CO3±„ŗĶČÜŅŗÖŠ³ÖŠųĶØČėCO2ĘųĢåÓŠ¹ĢĢåĪö³ö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
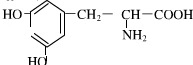 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Å£ÓĶ”¢ĻĖĪ¬ĖŲŗĶµ°°×ÖŹ¶¼ŹĒĢģČ»øß·Ö×Ó»ÆŗĻĪļ | |
| B£® | µķ·ŪĖ®½āµÄ×īÖÕ²śĪļŹĒĘĻĢŃĢĒ | |
| C£® | ĘĻĢŃĢĒÄÜ·¢ÉśŃõ»Æ·“Ó¦ŗĶĖ®½ā·“Ó¦ | |
| D£® | ÅØĮņĖį½¦ŌŚĘ¤·ōÉĻ£¬Ź¹Ę¤·ō³Ź»ĘÉ«ŹĒÓÉÓŚÅØĮņĖįŗĶµ°°×ÖŹ·¢ÉśĮĖŃÕÉ«·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŠĀÖĘĀČĖ®ÖŠÖ»ŗ¬Cl2ŗĶH2OĮ½ÖÖ·Ö×Ó | |
| B£® | ŠĀÖĘĀČĖ®æÉŹ¹×ĻÉ«ŹÆČļČÜŅŗĻȱäŗģŗóĶŹÉ« | |
| C£® | ¾ĆÖƵÄĀČĖ®pHŌö“ó£¬ĖįŠŌŌöĒæ | |
| D£® | ĀČĖ®¾¹āÕÕÓŠĘųÅŻŅŻ³ö£¬øĆĘųĢåŹĒCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŖĖŲÖÜĘŚ±ķÓŠ8øöÖ÷×å | B£® | 0×åŌ×ÓµÄ×īĶā²ćµē×ÓŹż¾łĪŖ8 | ||
| C£® | ¢ńA×åµÄŌŖĖŲČ«ŹĒ½šŹōŌŖĖŲ | D£® | ¶ĢÖÜĘŚŹĒÖøµŚ1”¢2”¢3ÖÜĘŚ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °±Ė® | B£® | ĒāŃõ»ÆÄĘ | C£® | ĖįŠŌøßĆĢĖį¼Ų | D£® | ŃĪĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe ĪŖÕż¼« | B£® | Cu ĪŖøŗ¼« | ||
| C£® | øŗ¼«ÉĻ·¢ÉśŃõ»Æ·“Ó¦ | D£® | Õż¼«ÉĻ·¢ÉśŃõ»Æ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com