
下列表示0.1 mol/L NaHCO3溶液中有关微粒浓度(mol/L)的关系式中,正确的是( )
A.c(Na+)>c(HCO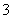 )>c(CO
)>c(CO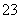 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.c(Na+)+c(H+)=c(HCO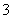 )+c(CO
)+c(CO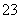 )+c(OH-)
)+c(OH-)
C.c(Na+)+c(H+)=c(HCO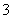 )+2c(CO
)+2c(CO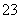 )+c(OH-)
)+c(OH-)
D.c(Na+)=c(HCO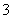 )+2c(CO
)+2c(CO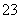 )+c(H2CO3)
)+c(H2CO3)
【解析】 在NaHCO3溶液中,除了H2O的电离外,还存在下列电离:
NaHCO3===Na++HCO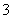 (完全电离)
(完全电离)
HCO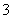 H++CO
H++CO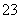 (只是微弱电离)
(只是微弱电离)
另外还存在水解反应:HCO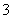 +H2OH2CO3+OH-。
+H2OH2CO3+OH-。
HCO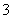 的水解程度也不大,但比HCO
的水解程度也不大,但比HCO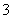 的电离程度大,故NaHCO3溶液呈碱性。在NaHCO3溶液中,碳原子的存在形式有HCO
的电离程度大,故NaHCO3溶液呈碱性。在NaHCO3溶液中,碳原子的存在形式有HCO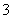 、CO
、CO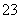 、H2CO3,其中以HCO
、H2CO3,其中以HCO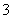 为主。由电荷守恒知,C项正确、B项不正确;由物料守恒知D项应为c(Na+)=c(HCO
为主。由电荷守恒知,C项正确、B项不正确;由物料守恒知D项应为c(Na+)=c(HCO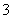 )+c(CO
)+c(CO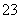 )+c(H2CO3),故D不正确。由于溶液呈碱性,且HCO
)+c(H2CO3),故D不正确。由于溶液呈碱性,且HCO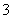 与H2O都能电离出H+,故A项应为:c(Na+)>c(HCO
与H2O都能电离出H+,故A项应为:c(Na+)>c(HCO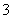 )>c(OH-)>c(H+)>c(CO
)>c(OH-)>c(H+)>c(CO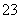 ),即A项错误。故选C。
),即A项错误。故选C。
【答案】 C


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验操作和现象描述以及解释均正确的是( )
| 操作和现象 | 解释 | |
| A | 向某卤代烃在碱性条件下水解后的溶液中滴加硝酸银溶液,有白色沉淀产生,证明该卤代烃是氯代烃。 | 因为氯代烃水解后的溶液中含Cl-,加入硝酸银溶液产生AgCl白色沉淀。 |
| B | 向溴水中加入苯充分振荡,静置分层,且水层几乎无色。 | 苯与溴水发生加成反应所以溴水褪色 |
| C | 要除去甲烷中混有的乙烯,可以将混合气体通入到酸性高锰酸钾溶液中,再通过浓硫酸干燥 | 因为乙烯可以被酸性高锰酸钾溶液氧化,而甲烷不能被氧化。 |
| D | 向蔗糖在酸性条件下水解的溶液中加NaOH溶液直至呈碱性,再加入新制的Cu(OH)2悬浊液,加热,产生砖红色沉淀。 | 说明蔗糖水解产生了葡萄糖。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
容积均为1 L的甲、乙两个恒容容器中,分别充入2 mol A、2 mol B和1 mol A、1 mol B,相同条件下,发生下列反应:A(g)+B(g)===xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法不正确的是( )
A.x=1
B.此条件下,该反应的平衡常数K=4
C.给乙容器升温可缩短反应达平衡的时间但不能提高平衡转化率
D.甲和乙中B的平衡转化率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为某化学反应速率—时间图像。在t1时刻升高温度和增大压强都符合下图所示变化的反应是( )

A.2SO2(g)+O2(g)2SO3(g) ΔH<0
B.4NH3(g)+5O2(g)4NO(g)+6H2O(g) ΔH<0
C.H2(g)+I2(g)2HI(g) ΔH>0
D.C(s)+H2O(g)CO(g)+H2(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)===3AlCl(g)+3CO(g) ΔH=a kJ·mol-1
3AlCl(g)===2Al(l)+AlCl3(g) ΔH=b kJ·mol-1
①反应Al2O3(s)+3C(s)===2Al(l)+3CO(g)的ΔH=________kJ·mol-1(用含a、b的代数式表示)。
②Al4C3是反应过程中的中间产物。Al4C3与盐酸反应(产物之一是含氢量最高的烃)的化学方程式为______________________________________________
___________________________________________________________________。
(2)镁铝合金(Mg17Al12)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为Mg17Al12+17H2===17MgH2+12Al。得到的混合物Y(17MgH2+12Al)在一定条件下可释放出氢气。
①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是________________________。
②在6.0 mol·L-1 HCl溶液中,混合物Y能完全释放出H2。1 mol Mg17Al12完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出H2的物质的量为________。
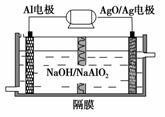
(3)铝电池性能优越,AlAgO电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为_________________________________________
_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应的能量变化如下图所示。下列有关叙述正确的是( )

A.该反应的反应热ΔH=E2-E1
B.a、b分别对应有催化剂和无催化剂的能量变化
C.催化剂能降低反应的活化能
D.催化剂能改变反应的焓变
查看答案和解析>>
科目:高中化学 来源: 题型:
环境监测测定水中溶解氧的方法是:
①量取a mL水样,迅速加入固定剂MnSO4溶液和碱性KI溶液(含KOH),立即塞好瓶塞,反复振荡,使之充分反应,其反应式为:2Mn2++O2+4OH-==2MnO(OH)2(该反应极快)。
②测定:开塞后迅速加入1~2 mL浓硫酸(酸化,提供H+),使之生成I2,再用b mol/L的Na2S2O3溶液滴定(以淀粉为指示剂),消耗V mL。有关反应式为:MnO(OH)2+2I-+4H+==Mn2++I2+3H2O、I2+2S2O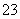 ==2I-+S4O
==2I-+S4O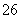 。
。
试回答:
(1)滴定过程中用到的玻璃仪器除了酸式滴定管、碱式滴定管外还缺少_____________________。
(2)滴定操作时,左手控制滴定管,右手________,眼睛要注视________。
(3)滴定(I2和S2O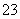 反应)以淀粉为指示剂,终点时溶液由________色变为________色。
反应)以淀粉为指示剂,终点时溶液由________色变为________色。
(4)水中溶解氧的计算式是______(以g/L为单位)。
(5)测定时,滴定管经蒸馏水洗涤后即加滴定剂Na2S2O3溶液,导致测定结果________(填“偏高”“偏低”或“无影响”,下同)。
(6)记录测定结果时,滴定前仰视刻度线,滴定到达终点时又俯视刻度线,将导致滴定结果________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在2 L密闭容器中把4 molA和2 mol B混合,在一定条件下发生反应3A(g)+2B(g)zC(g)+2D(g)。2 min后反应达到平衡时生成1.6 mol C,又测得反应速率v(D)=0.2 mol/(L·min)。则下列说法正确的是( )
A.z=4
B.B的转化率是20%
C.A的平衡浓度是1.6 mol/L
D.平衡时气体压强是原来的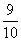
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com