
.卤代烃分子里的卤原子与活泼金属阳离子结合发生下列反应(X表示卤原子):
R—X+2Na+X—R′―→R—R′+2NaX
R—X+NaCN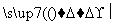 R—CN+NaX
R—CN+NaX
二烯烃可发生如下聚合反应:
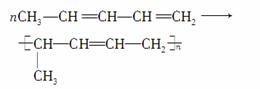
根据下列各物质的转化关系填空:
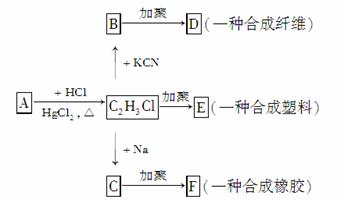
(1)A的分子式是__________,E的结构简式是________________。
(2)由B制备D的化学方程式__________________
________________________________________________________________________。
(3)由C制备F的化学方程式________________
________________________________________________________________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
.下列变化不属于取代反应的是
A. CH3COO C2H5+H2O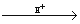 CH3COOH+ C2H5OH
CH3COOH+ C2H5OH
B. CH2= CH2+ H2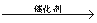 CH3 CH3
CH3 CH3
C. 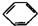 +HNO3
+HNO3
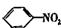 + H2O
+ H2O
D. CH4+ Cl2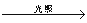 CH3Cl+HCl
CH3Cl+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物X能发生水解反应,水解产物为Y和Z,同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是( )
①乙酸丙酯 ②甲酸乙酯 ③乙酸甲酯 ④乙酸乙酯
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
某液态烃的分子式为C8H10,实验证明它能使酸性高锰酸钾溶液褪色,但不能使溴水褪色。
(1)试判断该有机物属于哪类烃,并写出其可能的同分异构体的结构简式。
(2)若苯环上的氢原子被溴原子取代,所得一溴代物有3种同分异构体,则该烃的结构简式为________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组制备消毒液(主要成分NaClO)设计了A、B两套装置。并查阅到下列资料,“在加热情况下卤素和碱液 发生如下反应3X2+6OH-
发生如下反应3X2+6OH-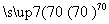 5X-+XO
5X-+XO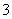 +3H2O”。
+3H2O”。

回答下列问题:
(1)装置A的大试管内发生反应的离子方程式为__________。
(2)装置A中能否省去盛饱和NaCl溶液的洗气瓶?________, 理由是___________。
(3)装置A中能否省去盛浓硫酸的洗气瓶? ,理由是____________。
(4)装置A中能否省去盛冰水的烧杯? ,理由是__________。
(5)装置B中制备Cl2时发生的电解反应的化学方程式为_____。
(6)装置B中a端应接电源的 极,理由是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是( )
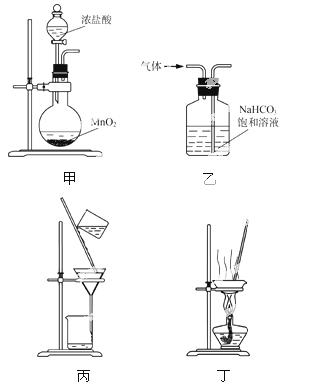
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl2·4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。理论上硫酸和硝酸的物质的量之比最佳为:
_________________________________。
(2)实际上,即使铜粉、硫酸及硝酸都比较纯,制得的CuSO4·5H2O中还是有可能存在的杂质是________,除去这种杂质的实验操作称为_____________________________。
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案甲:以空气为氧化剂。将铜粉在________(填仪器名称)中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案乙:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,即发生反应,生成硫酸铜。反应完全后,加物质甲调节pH,铁元素全部沉淀(一般认为铁离子的浓度下降到10-5 mol·L-1,就认为沉淀完全),然后过滤、浓缩、结晶。
请回答下列问题:已知:Ksp[Cu(OH)2]≈10- 22,Ksp[Fe(OH)2]≈10-16,Ksp[Fe(OH)3]≈10-38
22,Ksp[Fe(OH)2]≈10-16,Ksp[Fe(OH)3]≈10-38
①为了使铁元素全部沉淀,应调节pH至少为______________________________;
②甲物质可选用的是________;
A.CuCl2 B.NaOH C.Cu2(OH)2CO3 D.CuO E.H2SO4
③反应中加入少量FeSO4对铜的氧化可以起催化作用。其反应过程是:第1步,4Fe2++O2+4H+===4Fe3++2H2O,请写出其第2歩反应的离子方程式_____________________
________________________________________________________________________。
方案丙:将铜丝放到一定量的稀硫酸中,加入适量的H2O2,并控温在50 ℃~60 ℃,持续反应1 h,也能获得硫酸铜。请回答下列问题:
④反应时温度必须控制在50 ℃~60 ℃,温度不宜过高的主要原因是
________________________________________________________________________;
⑤写出该反应的化学方程式为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应不属于氧化还原反应的是( )
A.2F2+2H2O===4HF+O2 B.3CO+Fe2O3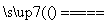 2Fe+3CO2
2Fe+3CO2
C.AgNO3+NaCl===AgCl↓+NaNO3 D.MgCl2(熔融)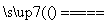 Mg+Cl2↑
Mg+Cl2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com