
以下进行性质比较的实验,不合理的是( )
|
| A. | 比较Cu、Fe2+的还原性:铁加入硫酸铜溶液中 |
|
| B. | 比较氯、溴单质的氧化性:溴化钠溶液中通入氯气 |
|
| C. | 比较镁、铝金属性:氯化镁、氯化铝溶液中分别加入过量的NaOH溶液 |
|
| D. | 比较碳、硫非金属性:测定同条件同物质的量浓度的Na2CO3、Na2SO4溶液的pH |
| 氧化性、还原性强弱的比较;金属在元素周期表中的位置及其性质递变的规律;非金属在元素周期表中的位置及其性质递变的规律.. | |
| 专题: | 实验设计题. |
| 分析: | A.根据还原剂的还原性强于还原产物的还原性分析; B.可通过单质之间的置换反应证明氧化性强弱,单质的氧化性越强; C.金属的最高价氧化物的水化物的碱性越强,金属的金属性越强; D.可根据对应最高价含氧酸对应的盐溶液的酸碱性判断酸性的强弱. |
| 解答: | 解:A.铁加入硫酸铜溶液中,生成铜,铁是还原剂,铜是还原产物,可以比较铁与铜的还原性强弱,不能比较Cu、Fe2+的还原性,故A错误; B.将氯气通入溴化钠溶液,生成单质溴,可证明氯气的氧化性比溴强,故B正确; C.氯化镁和氯化铝分别与氢氧化钠反应分别生成氢氧化镁沉淀和氢氧化铝沉淀,但氢氧化铝能溶于过量的氢氧化钠溶液中,氢氧化铝表现酸性,但氢氧化镁不能溶于氢氧化钠溶液中,说明氢氧化镁的碱性比氢氧化铝的碱性强,所以镁的金属性比铝强,故C正确; D.Na2CO3溶液呈碱性,说明碳酸为弱酸,Na2SO4溶液呈中性,说明硫酸为强酸,故D正确. 故选A. |
| 点评: | 本题考查非金属性与金属性、氧化性与还原性强弱比较的实验设计,难度不大,注意基础知识的理解掌握,注意选项C的理解. |


科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.雷雨时,可增加土壤中硝酸盐类氮肥的含量
B.许多领域中用液氮制得低温环境
C.造成光化学烟雾的罪魁祸首是SO2
D.正常雨水因溶有CO2,其pH约为5.6,而酸雨的pH小于5.6
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数,下列说法正确的是( )
A.22.4 L CO和CO2的混合气体中所含的碳原子数一定是NA
B.标准状况下22.4 L丙烷所含共用电子对数为8NA
C.常温常压下,32 g O2和32 g O3所含氧原子数都是2NA
D.常温下,1 L 0.1 mol·L-1 NH4NO3溶液中含有的NH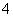 数是0.1NA
数是0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下, 质量为m的气体A与质量为n的气体B
质量为m的气体A与质量为n的气体B 的分子数相同,下列说法中不正确的是 ( )
的分子数相同,下列说法中不正确的是 ( )
A.气体A与气体B的相对分子质量比为m∶n
B.同质量气体A与气体B的分子个数比为n∶m
C.同温同压下,A气体与B气体的密度比为n∶m
D.相同状况下,同体积A气体与B气体的质量比为m∶n
查看答案和解析>>
科目:高中化学 来源: 题型:
异秦皮啶具有镇静安神抗肿瘤功效,秦皮素具有抗痢疾杆菌功效.它们在一定条件下可发生转化,如图所示.有关说法正确的是( )
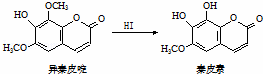
|
| A. | 异秦皮啶与秦皮素互为同系物 |
|
| B. | 异秦皮啶分子式为C11H12O5 |
|
| C. | 秦皮素一定条件下能发生加成反应、消除反应和取代反应 |
|
| D. | 1mol秦皮素最多可与2molBr2、4molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.
已知:SO2(g)+1/2O2(g)⇌SO3(g)△H=﹣98kJ•mol﹣1.
(1)某温度下该反应的平衡常数K=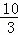 ,若在此温度下,向100L的恒容密闭容器中,充入3.0mol SO2(g)、16.0mol O2(g)和3.0mol SO3(g),则反应开始时v(正) v(逆)(填“<”、“>”或“=”).
,若在此温度下,向100L的恒容密闭容器中,充入3.0mol SO2(g)、16.0mol O2(g)和3.0mol SO3(g),则反应开始时v(正) v(逆)(填“<”、“>”或“=”).
(2)一定温度下,向一带活塞的体积为2L的密闭容器中充入2.0mol SO2和1.0mol O2,达到平衡后体积变为1.6L,则SO2的平衡转化率为 .
(3)在(2)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是 (填字母).
A.保持温度和容器体积不变,充入1.0mol O2
B.保持温度和容器内压强不变,充入1.0mol SO3
C.降低温度
D.移动活塞压缩气体
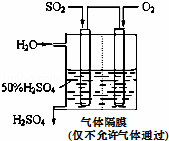
(4)若以如图所示装置,用电化学原理生产硫酸,写出通入O2电极的电极反应式为 .
(5)为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物PAS-Na是一种治疗肺结核药物的有效成分,有机物G是一种食用香料,以甲苯为原料合成这两种物质的路线如下:
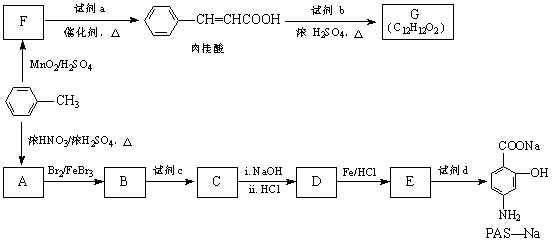

回答下列问题:
(1)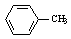 生成A的反应类型是 。
生成A的反应类型是 。
(2)F中含氧官能团的名称是 ;试剂a的结构简式为 。
(3)写出由A生成B的化学方程式: 。
(4)质谱图显示试剂b的相对分子质量为58,分子中不含甲基,且为链状结构,写出肉桂酸与试剂b生成G的化学方程式: 。
(5)当试剂d过量时,可以选用的试剂d是 (填字母序号)。
a.NaHCO3 b.NaOH c.Na2CO3
(6)写出C与NaOH反应的化学方程式 。
(7)肉桂酸有多种同分异构体,符合下列条件的有 种。
a.苯环上有三个取代基;
b.能发生银镜反应,且1 mol该有机物最多生成4 mol Ag。
由上述符合条件的同分异构体中,写出苯环上有两种不同化学环境氢原子的有机物的结构简式(任写一种即可) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,100 mL 0.01 mol·L-1的醋酸溶液与10 mL 0.1 mol·L-1的醋酸溶液相比较,下列数值前者大于后者的是( )
A.c(OH-) B.c(H+) C.中和时所需NaOH的量 D.c(CH3COOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com