
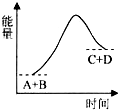
| A. | 是吸热反应 | |
| B. | 生成物的总能量高于反应物的总能量 | |
| C. | 只有在加热条件下才能进行 | |
| D. | 反应中断开化学键吸收的总能量高于形成化学键放出的总能量 |
分析 A.根据图象中反应物、生成物总能量大小判断吸热反应、放热反应;
B.根据图象可知该反应中反应物总能量低于生成物总能量;
C.反应条件与反应热没有必然关系,吸热反应不一定需要加热;
D.断裂化学键吸收能量,形成化学键放出能量,反应中断开化学键吸收的总能量高于形成化学键放出的总能量,即形成C、D键释放的总能量小于断A、B键吸收的总能量.
解答 解:A.根据图象曲线变化可知,反应物总能量低于生成物总能量,说明该反应为吸热反应,故A正确;
B.该反应为吸热反应,则生成物的总能量高于反应物的总能量,故B正确;
C.吸热反应不一定需要加热,如氯化铵与氢氧化钡晶体的反应为吸热反应,该反应不需要加热,故C错误;
D.该反应为吸热反应,断裂化学键吸收能量,形成化学键放出能量,则该反应中断开化学键吸收的总能量高于形成化学键放出的总能量,故D正确;
故选C.
点评 本题考查了反应热与焓变的应用,题目难度中等,根据图象曲线变化正确判断反应物、生成物总能量的关系为解答关键,注意掌握化学键键能变化与反应热的关系,试题有利于提高学生的分析、理解能力及灵活应用能力.


科目:高中化学 来源: 题型:推断题
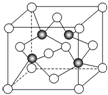 已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增.B原子的P轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3P轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体.根据以上信息,回答下列问题:
已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增.B原子的P轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3P轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体.根据以上信息,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内A、B、C的浓度之比为1:2:2 | |
| B. | 单位时间消耗0.2 mol/L B同时生成0.2 mol/L C | |
| C. | 容器内压强不随时间变化 | |
| D. | 容器内B的浓度不随时间变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
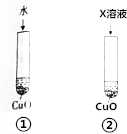 氧化铜可溶于稀硫酸,某同学为探究稀硫酸中的哪种粒子(H2O、H+、SO42-)使氧化铜溶解设计了如下实验.
氧化铜可溶于稀硫酸,某同学为探究稀硫酸中的哪种粒子(H2O、H+、SO42-)使氧化铜溶解设计了如下实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
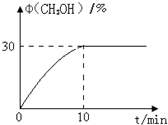 CO2加氢合成甲醇的技术,对减少温室气体排放和减缓燃料危机具有重要意义,发生的主要反应如下:CO2(g)+3H2(g)═CH3OH(g)+H2O(g).回答下列问题:
CO2加氢合成甲醇的技术,对减少温室气体排放和减缓燃料危机具有重要意义,发生的主要反应如下:CO2(g)+3H2(g)═CH3OH(g)+H2O(g).回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 由 CH3CH2OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1366.8 kJ•mol-1,可知乙醇的标准燃烧热为1366.8 kJ•mol-1 | |
| B. | 已知:C(金刚石,s)=C(石墨,s)△H<0,则金刚石比石墨稳定 | |
| C. | 已知:N2(g)+O2(g)═2NO(g)△H=+180 kJ•mol-1 2CO(g)+O2(g)═2CO2 (g)△H=-566 kJ•mol-1 则 2CO(g)+2NO(g)═N2 (g)+2CO2(g)△H=-746 kJ•mol-1 | |
| D. | OH-(aq)+H+(aq)═H2O(l)△H=-57.3 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠在氯气中燃烧产生黄色烟 | |
| B. | 锌和碘的混合粉末加几滴水有紫色气体产生 | |
| C. | 镁在空气中燃烧发出耀眼的白光 | |
| D. | 铜在氯气中燃烧产生棕黄色的烟 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com