
| A、淀粉、油脂、蛋白质都能水解,且水解产物各不相同 |
| B、从煤的干馏产物中可以获得焦炉气、粗氨水、煤焦油、焦炭等重要的化工原料 |
| C、石油催化裂化的主要目的是提高芳香烃的产量 |
| D、核酸是一类含磷的生物高分子化合物 |


科目:高中化学 来源: 题型:
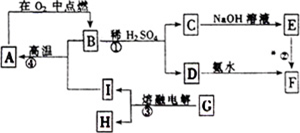
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平直接称量烧碱4.0g |
| B、在蒸发皿中灼烧CuSO4?5H2O晶体以除去结晶水 |
| C、用标准盐酸溶液滴定未知浓度的氨水,用酚酞作指示剂 |
| D、配制0.9%的氯化钠溶液时,将称量的氯化钠放入烧杯中加计量的水搅拌溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用干燥的蓝色石蕊试纸 |
| B、用干燥有色布条 |
| C、将气体通入AgNO3溶液 |
| D、用湿润的淀粉碘化钾试纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、22.4LNO气体中含有的分子数为NA |
| B、标准状况下,22.4LH2O中含有的水分子数为NA |
| C、常温常压下,11.2LH2中含有的氢分子数为0.5NA |
| D、在标准状况下22.4LCO中含有CO分子的个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 硫酸工业用SO2制取SO3的反应为:2SO2(g)+O2(g)
硫酸工业用SO2制取SO3的反应为:2SO2(g)+O2(g)| 催化剂 |
| 加热 |
| 温 度 | 200℃ | 300℃ | 400℃ |
| 平衡常数 | K1 | K2 | K3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com