


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:
| A、常温下pH=7的溶液中:Fe3+、Na+、Cl-、SCN- |
| B、常温下c(OH-)/c(H+)=1014的溶液中:K+、Mg2+、Cl-、Br- |
| C、含有大量HCO3-的澄清透明溶液中:K+、C6H5O-、Cl-、Na+ |
| D、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | ① | ② | ③ | 实验结论 | 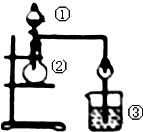 |
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
| D | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:C>Si |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应速率v(C)=1mol?L-1?s-1 |
| B、C的平衡浓度为4 mol?L-1 |
| C、A的转化率为25% |
| D、B的平衡浓度为1.5 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠和铁 | B、镁和铜 |
| C、铝和镁 | D、锌和铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
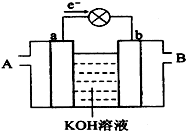 如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )
如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )| A、A处通入空气,B处通入水煤气 |
| B、a电极的反应式包括:CO+4OH--2e-=CO32-+2H2O |
| C、a电极发生还原反应,b电极发生氧化反应 |
| D、如用这种电池电镀铜,当镀件增重6.4g,则消耗标准状况下的水煤气4.48 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 微粒 | H+ | OH- | CH3COO- | CH3COOH |
| 物质的量浓度 | 减小 | 增大 | 增大 | 减小 |
| A、氯化氢 | B、氢氧化钠 |
| C、蒸馏水 | D、醋酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com