
���������(NH2COONH4)��һ�ְ�ɫ���壬�ֽ⡢��ˮ�⣬���������ϡ�������ϴ�Ӽ��ȡ�ij��ѧ��ȤС��ģ�ҵԭ���Ʊ���������泥���Ӧ�Ļ�ѧ����ʽ���£�2 NH3(g)+CO2(g)  NH2COONH4(s) ��H��0
NH2COONH4(s) ��H��0 
��1��ʵ�����Ʊ�NH3�Ļ�ѧ����ʽ�ǣ� ��
��2���Ʊ���������淋�װ������ͼ��ʾ���Ѱ����Ͷ�����̼ͨ�����Ȼ�̼�У����Ͻ����ϣ����ɵİ��������С�������������Ȼ�̼�С���������϶�ʱ��ֹͣ�Ʊ���
ע�����Ȼ�̼��Һ��ʯ����Ϊ���Խ��ʡ�
�ٷ������ñ�ˮ��ȴ��ԭ���� ��Һ��ʯ������ƿ�������� ��
�ڴӷ�Ӧ��Ļ�����з������Ʒ��ʵ�鷽���� (��д��������)��Ϊ�˵õ������Ʒ��Ӧ��ȡ�ķ����� (��дѡ�����)��
a. ��ѹ���Ⱥ�� b. ��ѹ���Ⱥ�� c. ���40 �����º��
��β������װ������ͼ��ʾ��˫ͨ�����ܵ����ã� ��
Ũ��������ã� �� �� ����������������
��3��ȡ�ֱ��ʶ�����̼����淋İ����������Ʒ0.7825 g��������ʯ��ˮ��ִ�����ʹ̼Ԫ����ȫת��Ϊ̼��ƣ����ˡ�ϴ�ӡ�����������Ϊ1.000 g������Ʒ�а�������淋����ʵ�������Ϊ ��
��1��2NH4Cl + Ca(OH)2��2NH3 ��+ CaCl2 + 2H2O(δд������1��)(2��)
��2���� �����¶ȣ���߷�Ӧ��ת����(���¶ȣ���ֹ��Ӧ������ɲ���ֽ�)(2��)��ͨ���۲����ݣ�����NH3��CO2ͨ�����(2��)�� ����(1��) c(1��)
�۷�ֹ����(2��)���ն��ఱ������ֹ������ˮ�������뷴Ӧ��ʹ���������ˮ��(2��)
��3��75%(3/4��0.75���������������)(3��)
���������������1��ʵ�����Ʊ�NH3�Ļ�ѧ����ʽ��2NH4Cl + Ca(OH)2 2NH3 ��+ CaCl2 + 2H2O��
2NH3 ��+ CaCl2 + 2H2O��
��2������Ϊ��Ӧ���ȣ������¶ȣ���߷�Ӧ��ת���ʣ�ͬʱ����ֹ��Ӧ������ɲ���ֽ⣻ͨ���۲����ݣ�����NH3��CO2ͨ������ڷ�Ӧ��Ĺ����Һ��Ļ����������Ʒ��ʵ�鷽���ǹ��ˡ���Ϊ������������ȶ��ԲΪ�˵õ������Ʒ��Ӧ��ȡ�ķ��������40 �����º�ɣ���ͼ��β������װ��ʹ���˽�����ϴ�IJ����ܣ��ɷ�ֹ������Ũ����������ն��ఱ������ֹ������ˮ�������뷴Ӧ��ʹ���������ˮ�⡣
��3����NH2COONH4����CaCO3��֪0.7825 g NH2COONH4��0.0133mol��1.000 g CaCO3��0.01mol����Ʒ�а�������淋����ʵ�������Ϊ75%��
���㣺��ѧʵ����ƺͲ�Ʒ���ȼ��㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
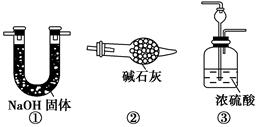
������ʵ��װ�ý��е�ʵ���У����ܴﵽ��Ӧʵ��Ŀ�ĵ���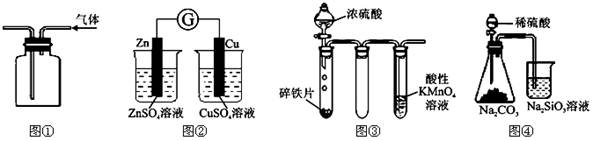
| A����ͼ����ʾʵ��װ���ſ������ռ�H2���� |
| B��ͼ��װ�ÿ���������֤��ѧ��ת��Ϊ���� |
| C��ͼ����Ƭ������ȫ�ܽ⣬�Ҹ��������Һ��ɫ |
| D��ͼ����ʾʵ��ɱȽ���̼��������Ԫ�صķǽ�����ǿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij����Һ����Ҫ�ɷ�ΪNaCl��NaClO���ڿ�����������CO2�����ʣ���NaCl��NaClO�����������¿ɷ�����Ӧ��ClO- + Cl- + 2H+ = Cl2��+ H2O��ijѧϰС����̽��������Һ�ı��������
��1��ȡ��������Һ�����Թ��У���������һ��Ũ�ȵ����ᣬ������ų���ͨ������װ�ü�������ijɷֿ����ж�����Һ�Ƿ���ʡ�
ѧϰС���о�����Ϊ����������������֣��ף����ֱ��ʣ��ң�δ���ʣ����� ��
Ϊ����֤����Ϊ�ף����������ʵ�鷽������ѡ�Լ���
��98%��Ũ���� ��1%��Ʒ����Һ ��1.0 mol��L-1��KI��������Һ ��1.0 mol��L-1 ��NaOH��Һ �ݳ���ʯ��ˮ �ޱ���NaCl��Һ
| �����Լ� | Ԥ������ͽ��� |
| �Թ�A�м����� ������ţ��� �Թ�B�м�1%Ʒ����Һ�� �Թ�C�м� ������ţ��� | ��___ ___�� ��׳����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��14�֣�̼��þ������һ�����͵��������β����е���ǿ���ϡ�
(1)�ϳɸ����ʵIJ������£�
����1������0.5 mol��L��1MgSO4��Һ��0.5 mol��L��1NH4HCO3��Һ��
����2������Ͳ��ȡ500 mL NH4HCO3��Һ��1 000 mL������ƿ�У��������������¶ȿ�����50 �档
����3����250 mL MgSO4��Һ��μ���NH4HCO3��Һ�У�1 min�ڵμ�����ð�ˮ������ҺpH��9.5��
����4������1 h���ˡ�ϴ�ӡ�
����5����40 �����ո������и���10 h����̼��þ�����Ʒ(MgCO3��nH2O��n��1��5)��
�ش��������⣺
����3�мӰ�ˮ������ӷ���ʽ ��
(2)�ⶨ�ϳɵ�MgCO3��nH2O�е�nֵ������1.000 g̼��þ���룬������ͼ��ʾ�Ĺ��ƿ�м���ˮ����ϡ�����뾧�뷴Ӧ�����ɵ�CO2��NaOH��Һ���գ��������·�Ӧ4��5 h����Ӧ���ڽ��¶�����30 �棬�����ձ��е���Һ����֪Ũ�ȵ�����ζ������CO2���������ظ���������2�Ρ�

��ͼ������������� ��
��������Ӧ����Ҫ���µ�30�棬��ҪĿ���� ��
������֪Ũ�ȵ�����ζ��ձ��е���ҺʱӦѡ�� Ϊָʾ������ʢ������ĵζ����ڵζ�ǰ������δ�ž����ζ��������ݣ�������������ȷ����������CO2������ ���ƫ��ƫС������Ӱ�족��
����3��ʵ����ÿ1.000 g̼��þ������ϡ���ᷴӦ������CO2ƽ��ֵΪa mol����nֵΪ (�ú�a�ı���ʽ��ʾ)��
(3)��ȡ100 g���������Ʒ�������ط���������������ͼ����������ºϳɵľ����У�n�� (ѡ��1��2��3��4��5)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��13�֣������������һ����Ҫ�Ļ�����Ʒ��ij��ȤС�����Ʊ���������ƾ��壨Na2S2O3��5H2O����
I��[��������]
��1��Na2S2O3��5H2O����ɫ�����壬������ˮ����ϡ��Һ��BaCl2��Һ����������ɡ�
��2����Na2CO3��Na2S���Һ��ͨ��SO2���Ƶ�Na2S2O3�����ò�Ʒ�г���������Na2SO3��Na2SO4��
��3��Na2SO3�ױ�������BaSO3������ˮ��������ϡHCl��
��.[�Ʊ���Ʒ]
ʵ��װ����ͼ��ʾ��ʡ�Լг�װ�ã�
ʵ�鲽�裺
��1�����װ�������ԣ���ͼʾ�����Լ�������a��������____��E�е��Լ���___��ѡ��������ĸ��ţ���
A��ϡH2SO4 B��NaOH��Һ C������NaHSO3��Һ
��2������C����ƿ����Na2S��Na2CO3�����Һ������A����ƿ�μ�ŨH2SO4��
��3����Na2S��Na2CO3��ȫ���ĺ�����Ӧ������C�л��Һ����Һ��____����д�������ƣ����ᾧ�����ˡ�ϴ�ӡ�����õ���Ʒ��
��[̽���뷴˼]
��1��Ϊ��֤��Ʒ�к���Na2SO3��Na2SO4����С�����������ʵ�鷽�����뽫���������������������Լ���ϡHNO3��ϡH2SO4��ϡHCl������ˮ��ѡ��
ȡ������Ʒ���ϡ��Һ���μ�����BaCl2��Һ���а�ɫ�������ɣ�_____��������δ��ȫ�ܽ⣬���д̼�����ζ��������������ȷ����Ʒ�к���Na2SO3��Na2SO4��
��2��Ϊ����װ��C�����ɵ�Na2SO4�������ڲ��ı�ԭ��װ�õĻ����϶�ԭ��ʵ�鲽�裨2�������˸Ľ����Ľ���IJ�����_______��
��3��Na2S2O3��5H2O���ܽ�����¶����������������ò�Ʒͨ��_____�����ᴿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��14�֣�ijͬѧ��ͼʾװ�ý�������ϡ���ᷴӦ��ʵ�鲢������ص�ʵ��̽����
a������ƿ��ע��������NaOH��Һ����ʢ��һ�������Ĵ����۵�С�ձ�����ƿ�С�
b���ر�ֹˮ�У���ȼ���ף�����ƿ�У����ý�����
c�������׳��ȼ�գ�һ��ʱ����Һ©�����������ձ��л�������һ������4mol��L��1��ϡ���ᣬ
������ȫ�ܽ⡣
��һ���������ɷ�̽��
��1��ʵ��ǰ��μ���װ�õ������ԣ� ��
��2��ȼ�պ���Ŀ���� ��
��3��Ϊ֤���������ΪNO������c��ȱ�ٵ�һ����Ҫ������ ��
��������������Ԫ�ؼ�̬̽����
��1������������裺
����1��������ֻ��+2����������2�� ������3�������м���+2����������+3������
��2�����ʵ�鷽������֤����1������д��ʵ��������衢����ͽ��ۣ��� ��
��������������
��1�����ƿ����NaOH��Һ����Ҫ������ ��
��2��������3��������������Һ��n(Fe2+)��n(Fe3+)=3��1ʱ�����Ӧ�����ӷ�Ӧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
(15 ��)
������ͭ�Ǻϳ��������������в��ϡ�����������ͭ����Ҫǰ����֮һ������������һ��ʵ���Һϳ�·�ߣ�
�Ʊ��������װ��ʾ��ͼ����(���Ⱥͼг�װ�õ���)��
��֪����������۵�Ϊ76.5 �棬������ˮ�������Ҵ���
�ش��������⣺
��1����250 mL����ƿa�м���70 mL70%���ᡣ���ƴ�����ʱ����������ˮ��Ũ������Ⱥ�˳����
��
��2����a�е���Һ������100 �棬�����μ�40 g�����浽������Һ�У�Ȼ��������130 �������Ӧ����װ���У�����b�������� ������c�������� ���������� ��
��Ӧ�������������ˮ���ٷ�����������Ʒ��������ˮ��Ŀ���� �����������п����ڷ��뱽�����Ʒ���� (����)��
| A����Һ©�� | B��©�� | C���ձ� | D��ֱ��������E�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��ͼ��ʾ���ϳɰ�������ʾʵ��(�г���������ʡ��)����Y�ιܵ�һ����Zn����ϡH2SO4��Ӧ��ȡH2����һ����NaNO2�����NH4Cl������Һ��Ӧ��ȡN2��N2��H2��Ϻ�ͨ����ԭ�������ϳ�NH3���ٽ�����������ͨ���̪��Һ�У�����̪��Һ��죬��˵�������˰�����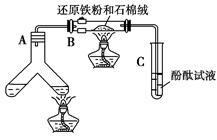
ij����С��ͨ���������ϺͶ��ʵ�飬�õ���������Ϣ��
��Ϣһ��NaNO2����ͱ���NH4Cl��Һ��ϼ��ȵĹ����з������·�Ӧ��
��NaNO2��NH4Cl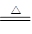 NH4NO2��NaCl
NH4NO2��NaCl
��NH4NO2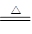 NH3����HNO2
NH3����HNO2
��2HNO2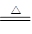 N2O3����H2O
N2O3����H2O
��2NH3��N2O3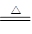 2N2��3H2O
2N2��3H2O
��Ϣ�����������ϣ���ͬ����ȵ�N2��H2�����������ͬʵ�������ºϳɰ���ʹ��̪��Һ�������Ҫ��ʱ�����£�
| N2��H2������� | 5��1 | 3��1 | 1��1 | 1��3 | 1��5 |
| ��̪���ɫ����ʱ��/min | 8��9 | 7��8 | 6��7 | 3��4 | 9��10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��ˮ����ͭ��ǿ���»ᷢ���ֽⷴӦ��
CuSO4  CuO + SO3�� 2SO3
CuO + SO3�� 2SO3  2SO2��+ O2��
2SO2��+ O2��
����ͼ��ʾװ�ã��г���������ȥ��������D���ڷ�Ӧǰ��������������ֽ��˵���ˮ����ͭ��������
ʵ�鲽�裺
�ٳ�����ӦǰD�ܵ�������
�����Ӻ�װ�ã��ر�K������Ӳ�ʲ�����Aһ��ʱ���ֹͣ���ȡ�
�۴�Ӳ�ʲ�����A��ȴ��K��ͨ��һ��ʱ����ѳ�ȥ������̼����������Ŀ�����
���ٳ���D�ܣ����䷴Ӧǰ���������Ϊm��
�ش��������⣺
��1����Ӧ2SO3(g)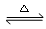 2SO2(g) + O2(g)��ƽ�ⳣ������ʽΪK= ��
2SO2(g) + O2(g)��ƽ�ⳣ������ʽΪK= ��
��2��B���г��¶����������⣬���ɿ����������� �����¶��������ߵ���Ҫԭ���� ��B���з�����Ӧ���й����ӷ���ʽ�� ��
��3������E�������� ��
��4������������ʵ�飬����B��C��D����������վ���ȫ�������Կ�����CO2��Ӱ�죬�ܷ����m������ֽ��˵���ˮCuSO4��������(��ѡ��һ�ش�)
������ܣ���ֽ����ˮCuSO4������Ϊ ����m��ʾ����
��������ܣ���ԭ���� ��Ϊ���ܲ�÷ֽ��˵���ˮ����ͭ����������ļ�ʵ�鷽���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com