
| A | B | C | D | E |
| ①是一种烃,能使溴的四氯化碳溶液褪色 ②比例模型为:  ③能与水在一定条件下反应生成C | ①由C、H两种元素组成 ②球棍模型为: 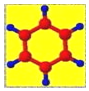 | ①能与钠反应,但不能与NaOH溶液反应; ②能与E反应生成相对分子质量为100的酯 | ①由C、H、Br三种元素组成; ②相对分子质量为109 | ①由C、H、O三种元素组成; ②球棍模型为: 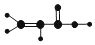 |
 ;
;分析 A使溴的四氯化碳溶液褪色,含有不饱和键,结合其比例模型可知,A为CH2=CH2,A能与水在一定条件下反应生成C,C由C、H、O三种元素组成,能与Na反应,但不能与NaOH溶液反应,故C为CH3CH2OH,根据B的组成元素及其球棍模型知,B是苯.结构简式为 ;D由C、H、Br三种元素组成,相对分子质量为109,所以D是CH3CH2Br;E由C、H、O三种元素组成,E和C反应生成相对分子质量为100的酯,说明E含有羧基,结合E的球棍模型可知E为CH2=CHCOOH,以此解答该题.
;D由C、H、Br三种元素组成,相对分子质量为109,所以D是CH3CH2Br;E由C、H、O三种元素组成,E和C反应生成相对分子质量为100的酯,说明E含有羧基,结合E的球棍模型可知E为CH2=CHCOOH,以此解答该题.
解答 解:(1)A为CH2=CH2,乙烯和溴发生的化学反应为:CH2=CH2+Br2→CH2BrCH2Br,故答案为:CH2=CH2+Br2→CH2BrCH2Br;
(2)A与氢气发生加成反应后生成物质F为乙烷,当烷烃中碳原子数目为4时开始出现同分异构体,故答案为:4;
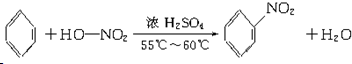
(3)B是苯,结构简式为 ,分子式为C6H6,与浓硝酸反应的化学方程式:
,分子式为C6H6,与浓硝酸反应的化学方程式: ,
,
故答案为:C6H6; ;
;
(4)C与E反应的反应类型为取代反应,反应方程式为:CH2=CHCOOH+CH3CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOOCH2CH3+H2O,
故答案为:CH2=CHCOOH+CH3CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOOCH2CH3+H2O.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,熟悉常见有机物官能团及其性质,熟悉常见有机反应类型,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=C(CH3) CH3 3-甲基-2-丁烯 | |
| B. | CH3CH(CH3)CH(Cl)CH3 3-甲基-2-氯丁烷 | |
| C. | CH3CH(OH)CH2CH3 3-羟基丁醇 | |
| D. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,能说明O元素比N元素为非金属强的是氧气与氢气化合更容易,生成的水比氨气更稳定,其中三种主族元素的离子半径从大到小的顺序是N3->O2->Na+(用离子符号表示).
,能说明O元素比N元素为非金属强的是氧气与氢气化合更容易,生成的水比氨气更稳定,其中三种主族元素的离子半径从大到小的顺序是N3->O2->Na+(用离子符号表示).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C、N、O元素的单质与氢气化合越来越难 | |
| B. | Li、Na、K的氧化物的水化物的碱性依次减弱 | |
| C. | Na、Mg、Al的简单离子的氧化性以依次增强 | |
| D. | P、S、Cl元素的最高正价依次升高,其对应的气态氢化物的稳定性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜插入浓硝酸中:Cu+4H++2NO3?═Cu2++2NO2↑+2H2O | |
| B. | 向FeBr2溶液中通入过量氯气:2Fe2++Cl2═2Fe3++2Cl? | |
| C. | 向Al2O3中加入氨水:Al2O3+2OH?═2AlO2?+H2O | |
| D. | 碳和浓硫酸加热:C+2H++SO42?═H2O+SO2↑+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com