
为了测定酸碱反应的中和反应反应热,计算时至少需要的数据是 ( )
①酸的浓度和体积 ②碱的浓度和体积 ③比热容 ④反应后溶液的质量
⑤生成水的物质的量 ⑥反应前后溶液温度变化 ⑦操作所需的时间
A.①②③⑥ B.①③④⑥ C.③④⑤⑥ D.全部
 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 乙醇燃烧是生成物总能量高于反应物总能量的反应。
B. 稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol可表示稀硫酸与稀Ba(OH)2溶液反应的中和热为ΔH=-57.3 kJ/mol。
C. 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H=―Q kJ/mol可以表示H2S的燃烧热。
D. 高温下,某反应达到平衡,平衡常数为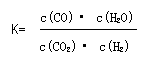
恒容时,温度升高,H2浓度减小,故该反应的焓变为正值。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列说法正确的是( )
A. 1 mol·L—1 Na2CO3溶液中的CO32-数目为NA
B. 标准状况下,11.2L H2O中含有的电子数目为5NA
C. 1 mol Na与足量O2反应生成Na2O或Na2O2失去电子数目均为NA
D. 2.7g金属铝无论与强碱还是强酸作用时失去电子数目均为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
据《自然》杂志报道,在300~400℃的高温下,将砂糖(主要成分为蔗糖)等碳水化合物用加热的方法使其形成焦糖与碳之间的“半成品碳”状态,再放进硫酸溶液中高温加热,生成了一种叫“焦糖烯”的物质,其分子式为C36H50O25。下列有关说法正确的是
A.“半成品碳”在硫酸溶液中加热可能发生的是消去反应
B.“半成品碳”是碳元素的一种新单质
C. 蔗糖溶液与新制的氢氧化铜悬浊液混合加热有砖红色沉淀生成
D. 焦糖烯是一种新型的烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生
产中保持恒温恒容条件):
2SO2(g)+O2 (g) 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1
⑴生产中为提高反应速率和SO2的转化率,下列措施可行的是
A.向装置中充入N2 B.向装置中充入过量的SO2
C.向装置中充入O2 D.升高温度
⑵若在一定温度下,向一个容积可变的恒压容器中,通入3mol SO2 和2mol O2 及
固体催化剂,发生上述反应,平衡时容器内气体体积为起始时的90%。保持同一
反应温度,在相同容器中,将起始物质的量改为 5mol SO2(g) 、3.5 mol O2
(g) 、1mol SO3 (g) ,下列说法正确的是
A.第一次平衡时反应放出的热量为294.9kJ
B.两次平衡SO2的转化率相等
C.两次平衡时的O2体积分数相等
 D.第二次平衡时SO3的体积分数等于2/9
D.第二次平衡时SO3的体积分数等于2/9
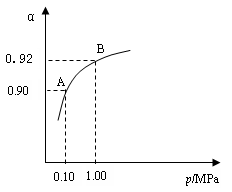
⑶生产中在550 ℃时,将2.0 mol SO2和1.0 mol O2置于5 L密闭容器中,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如右图所示。反应达平衡后,体系总压强为0.10 M Pa。试计算反应2SO3 2SO2+O2 在550 ℃时的平衡常数K= 。
2SO2+O2 在550 ℃时的平衡常数K= 。
A、B表示不同压强下的平衡转化率,通常工业生产中采用常压的原因是: ,并比较不同压强下的平衡常数:K(0.10 MPa)
K(1.0 MPa)(填 “<”或“>”或“=”)。
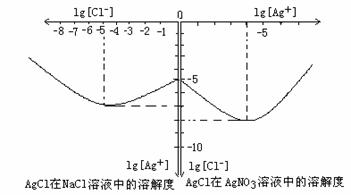 ⑷沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。已知AgCl + Cl- = [AgCl2]-, 右图是某温度下AgCl在NaCl溶液中的溶解情况。由以上信息可知:
⑷沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。已知AgCl + Cl- = [AgCl2]-, 右图是某温度下AgCl在NaCl溶液中的溶解情况。由以上信息可知:
①由图知该温度下AgCl的溶度积常数为 。
②AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:
查看答案和解析>>
科目:高中化学 来源: 题型:
充分燃烧一定量丁烷时放出的热量xQ,完全吸收它生成的CO2生成正盐,需5mol/L的KOH溶液100ml,则丁烷的燃烧热为( )
A.16xQ B.8xQ C.4xQ D.2xQ
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1 mol时,下列说法不正确的是( )。
A.溶液的质量变化:甲减小乙增大
B.溶液pH变化:甲减小乙增大
C.相同条件下产生气体的体积:V甲=V乙
D.电极反应式:甲中阴极为Cu2++2e-===Cu,
乙中负极为Mg-2e-=== Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
C、O、Na、Al、S、Cl是常见的六种元素
(1)C元素位于元素周期表第 周期,第 族;C元素的一种同位素可以测定文物年代,这种同位素的符号为
(2)用“大于”“小于”或“等于”填空
| 离子半径 | 酸性 | 还原性 | 得电子能力 |
| N3- Al3+ | H2SO4 HClO4 | O2- S2- | 35Cl 37Cl |
(3)① CaCO3和适量HCl溶液反应时,每产生4.4 g 气体(不考虑气体溶解),放热a kJ,则该反应的热化学方程式为 。
②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得pH变化曲线如图所示

请用离子方程式表示B-C段发生的反应:
(4)氢气、氧气常用来作燃料电池,写出电解质为氢氧化钠溶液时
负极上的电极方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com