
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在________部分发生反应,在________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为:_____________;
加入硅、锰和铝的目的是____________。
(3)不锈钢含有的 Cr 元素是在炼钢过程的氧吹________(填“前”或“后”)加入,原因是_________________。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_____。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
)(1)常温下,将0.2 mol/L HCl溶液与0.2 mol/L氨水等体积混合(忽略混合后溶液体积的变化),测得混合后溶液的pH=6,试回答以下问题:
(1)混合后溶液呈酸性的原因是(用离子方程式回答) 。
(2)混合后溶液中由水电离出的c(OH-)为
(3)常温下,将0.2 mol·L-1的盐酸与 0.2mol·L-1的氨水混合,若所得的混合溶液中的pH=7,下列关系正确的是
A、[Cl-]>[NH4+]> [H+] > [OH-] B、[NH4+]>[Cl-]>[OH-]>[H+]
C、[Cl-]=[NH4+]>[H+]=[OH-] D、[NH4+]>[Cl-]>[H+]>[OH-]
(4)由电离常数可知酸性强弱: CH3COOH>H2CO3>HCO3-,则浓度相同的下列溶液碱性由强到弱顺序为: (填序号)
①CH3COONa ② NaHCO3 ③ Na2CO3
(5)将氯化铁溶液蒸干、灼烧,最后得到的固体是 。
(6)Cu(OH)2(s) 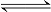 Cu2+(aq)+2OH-(aq),在常温下Ksp( Cu(OH)2)=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol•L-1的CuSO4溶液中加入NaOH溶液,调整pH最小到 。
Cu2+(aq)+2OH-(aq),在常温下Ksp( Cu(OH)2)=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol•L-1的CuSO4溶液中加入NaOH溶液,调整pH最小到 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语使用正确的是
A.NH4Br的电子式: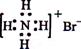 B.S2-的结构示意图:
B.S2-的结构示意图:
C.乙酸的分子式: CH3COOH D.原子核内有l8个中子的氯原子: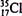
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是宝贵的自然资源,从海水中可以提取多种化工原料,如图是某工厂对海水综合利用的示意图:
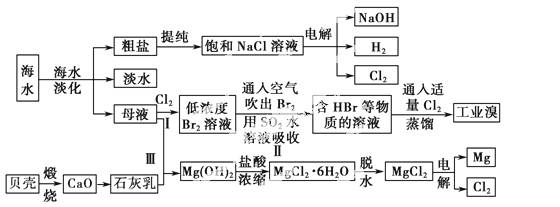
(1)在粗盐中含有Ca2+、Mg2+、SO等杂质,电解精制时所用的试剂有①盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。则加入试剂的先后顺序是____________(填编号)。
(2)工业上电解饱和食盐水的离子方程式:_________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是____________ _____。
_____。
步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式:_____________________。
(4)从步骤Ⅲ得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是向沉淀中加入________溶液,充分搅拌后经________(填操作方法)可得纯 净的Mg(OH)2。
净的Mg(OH)2。
(5)在制取无水氯化镁时需要在干燥的HCl气流中加热MgCl2·6H2O的原因:______________________。
(6)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气冷却剂的是________(填序号)。
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7)。工艺流程及相关物质溶解度曲线如图
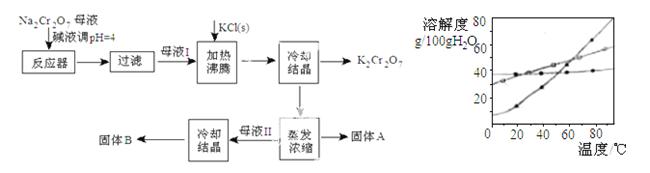 (1)由Na2Cr2O7生产K2Cr2O7的化学方程式为
(1)由Na2Cr2O7生产K2Cr2O7的化学方程式为  。通过冷过结晶析出大量K2Cr2O7的原因是 。
。通过冷过结晶析出大量K2Cr2O7的原因是 。
(2)向Na2Cr2O7母液中加碱液调pH的目的是 。
(3)固体A主要为 (填化学 式)
式) ,固体B主要为 (填化学式)。
,固体B主要为 (填化学式)。
(4)用热水洗涤固体A,回收的洗涤液转移到母液 (填“I”“II”或“III”)中,既能提高产率又可使能耗最低。
查看答案和解析>>
科目:高中化学 来源: 题型:
美国科学家理查德·海克和日本科学家根岸英一、铃木彰因在研发“有机合成中的钯催化的交叉偶联”而获得2010年度诺贝尔化学奖。有机合成常用的钯/活性炭催化剂,长期使用催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,需对其再生回收。一种由废催化剂制取氯化钯的工艺流程如下:
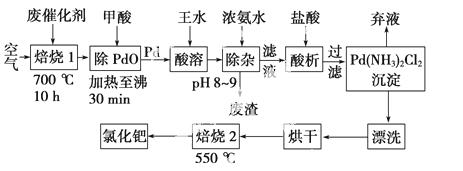
(1)废钯催化剂经烘干后,再在700 ℃的高温下焙烧,焙烧过程中需通入足量空气的原因是________________________________________________________________________;
甲酸还原氧化钯的化学方程式为____________________ ______________________。
______________________。
(2)钯在王水(浓硝酸与浓盐酸按体积比1∶3)中转化为H2PdCl4,硝酸还原为NO,该反应的化学方程式为______________________。
(3)钯精渣中钯的回收率高低主要取决于王水溶解的操作条件,已知反应温度、反应时间和王水用量对钯回收率的影响如下图1~图3所示,则王水溶解钯精渣的适宜条件(温度、时间和王水用量)为__________、__________、__________。
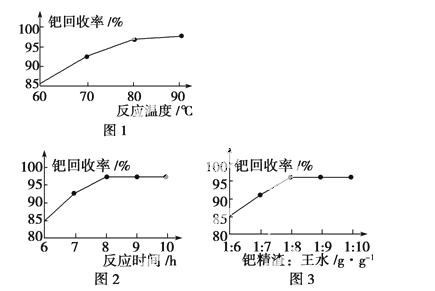
(4)加浓氨水时,钯转变为可溶性[Pd(NH3)2]2+,此时铁的存在形式是________________________________________________________________________(写化学式)。
(5)700 ℃焙烧1的目的是________________;550 ℃焙烧2的目的是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
右图模 拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是
拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是
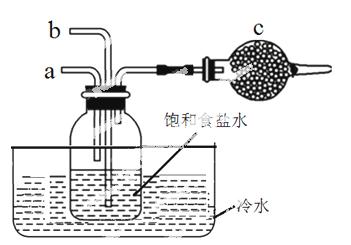
A.a通入CO2,然后b通入NH3,c中放碱石灰
B.b通入NH3,然后a通入CO2,c中放碱石灰
C.a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D.b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是常见的不同主族的短周期元素,它们的原子序数逐渐增大。已知其中只有一种是金属元素,C元素原子最外层电子数是D元素原子的最外层电子数的一半,B元素原子的最外层电子数比D元素原子的最外层电子数少2个。E、F也是短周期元素,E与D同主族,F与A同主族。
(1)写出F2E2的电子式:_____________________,
其晶体类型为________,其化学键类型为____________________。
(2)E与D各自形成的氢化物中沸点较高的是____ ____(填化学式),其原因是___________________________,
____(填化学式),其原因是___________________________,
A与B所形成最简单化合物的结构式为________,空间构型为________。
(3)六种元素中的三种组成的易溶于水的酸性物质中,能促进水电离的物质M是___________________
(写化学式,写一个 即可,下同),能抑制水电离的物质N是________。
即可,下同),能抑制水电离的物质N是________。
25 ℃时,pH=a的M溶液中由水电离出的H+浓度与pH=a的N溶液中由水电离出的H+浓度之比为________。
(4)甲、乙、丙分别是B、C、D三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,且丙的用量不同,反应的产物不同。回答下列问题:
①向乙溶液中缓慢滴加过量的丙溶液,过程中发生反应的离子方程式为___________________。
②向甲溶液中缓慢滴加过量的丙溶液,所观察到的实验现象为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com