
”¾ĢāÄæ”æ”°ÉńŹ®“īŌŲµÄ³¤Õ÷FøĽųŠĶ»š¼żĶĘ½ų¼ĮÖ®Ņ»ĪŖĪŽÉ«ĘųĢåN2O4£¬N2O4ÓėNO2×Ŗ»»µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗN2O4(g)![]() 2NO2(g) ”÷H=+24.4KJ/mol
2NO2(g) ”÷H=+24.4KJ/mol
(1)½«Ņ»¶ØĮæN2O4Ķ¶Čė¹Ģ¶ØČŻ»żµÄÕęæÕČŻĘ÷ÖŠ£¬ĻĀŹöĻÖĻóÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāµÄŹĒ ”£
a£®vÕż(N2O4)=2vÄę(NO2) b£®ĢåĻµŃÕÉ«²»±ä
c£®ĘųĢåĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»±ä d£®ĘųĢåĆÜ¶Č²»±ä
“ļµ½Ę½ŗāŗ󣬱£³ÖĢå»ż²»±äÉżøßĪĀ¶Č£¬ŌŁ“Īµ½“ļĘ½ŗāŹ±£¬Ōņ»ģŗĻĘųĢåŃÕÉ« (Ģī”°±äÉī”±”¢”°±äĒ³”±»ņ”°²»±ä”±)£¬ÅŠ¶ĻĄķÓÉ ”£
£Ø2)T”ꏱ£¬Ļņ1LŗćČŻĆܱÕČŻĘ÷ÖŠĶ¶Čė1molCH4ŗĶ1molH2O(g)£¬·¢Éś·“Ó¦£ŗCH4(g)+H2O(g)![]() CO(g)+3H2(g)£¬¾¹ż3min£¬·“Ó¦“ļµ½Ę½ŗā”£ŅŃÖŖĘ½ŗāŹ±c(CH4)=0.5mol/L
CO(g)+3H2(g)£¬¾¹ż3min£¬·“Ó¦“ļµ½Ę½ŗā”£ŅŃÖŖĘ½ŗāŹ±c(CH4)=0.5mol/L
¢Ł0”«3minÄŚ£¬øĆ·“Ó¦µÄĘ½¾ł·“Ó¦ĖŁĀŹv(H2)=____________”£
¢ŚT”ꏱ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżK=___________”£
(3)ŌŚŅ»¶ØĢõ¼žĻĀÓĆCOŗĶH2æÉŅŌÖĘµĆ¼×“¼£¬CH3OHŗĶCOµÄČ¼ÉÕČČĪŖ±š725.8 kJ/mol £¬283.0 kJ/mol£¬1 molŅŗĢ¬Ė®±ä³ÉĘųĢ¬Ė®ĪüČČ44.0 kJ£¬Š“³ö¼×“¼²»ĶźČ«Č¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼ŗĶĘųĢ¬Ė®µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
(4)¹¤ŅµÉĻÓĆCOÓėH2ŌŚ“߻ƼĮ×÷ÓĆĻĀŗĻ³ÉCH3OH,Ęä·“Ó¦ĪŖ£ŗCO(g)+2H2(g)![]() CH3OH(g)”£°“n(CO) : n(H2)=1 : 2ĻņĆܱÕČŻĘ÷ÖŠ³äČė·“Ó¦Īļ£¬²āµĆĘ½ŗāŹ±»ģŗĻĪļÖŠCH3OHµÄĢå»ż·ÖŹżŌŚ²»Ķ¬Ń¹ĒæĻĀĖęĪĀ¶ČµÄ±ä»ÆČēĶ¼ĖłŹ¾”£
CH3OH(g)”£°“n(CO) : n(H2)=1 : 2ĻņĆܱÕČŻĘ÷ÖŠ³äČė·“Ó¦Īļ£¬²āµĆĘ½ŗāŹ±»ģŗĻĪļÖŠCH3OHµÄĢå»ż·ÖŹżŌŚ²»Ķ¬Ń¹ĒæĻĀĖęĪĀ¶ČµÄ±ä»ÆČēĶ¼ĖłŹ¾”£
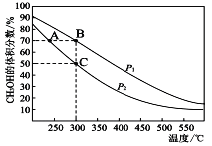
P1_________P2(Ģī”°<”±”°>”±»ņ”°=”±)
¢ŚŌŚCµćŹ±£¬CO×Ŗ»ÆĀŹĪŖ____________”£
”¾“š°ø”æ(15·Ö)(1)bc(2·Ö)£»±äÉī(1·Ö)Õż·“Ó¦ŹĒĪüČČ·“Ó¦£¬ĘäĖūĢõ¼ž²»±ä£¬ĪĀ¶ČÉżøßĘ½ŗāÕżĻņŅĘ¶Æ£¬c(NO2)Ōö¼Ó£¬ŃÕÉ«¼ÓÉī(2·Ö)
(2)¢Łv(H2)=0.5moL/(L”¤min)(2·Ö)£¬¢ŚK=6.75(mol/L)2(2·Ö)
(3)CH3OH(l)£«O2(g)=CO(g)£«2H2O(g)¦¤H=-354.8kJØMmol(2·Ö)
(4)¢Ł>(2·Ö)£¬¢Ś75%(2·Ö)
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ(1)a£®Ó¦ŹĒ2vÕż(N2O4)=vÄę(NO2) Ź±·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹Źa“ķĪó£»b£®ĢåĻµŃÕÉ«²»±ä£¬ĖµĆ÷¶žŃõ»ÆµŖÅØ¶Č²»±ä£¬·“Ó¦µ½“ļĘ½ŗāדĢ¬£¬¹ŹbÕżČ·£»c£®»ģŗĻĘųĢå×ÜÖŹĮæ²»±ä£¬Ėę·“Ó¦¼õŠ”»ģŗĻĘųĢå×ÜĪļÖŹµÄĮæŌö“ó£¬Ę½¾łĻą¶Ō·Ö×ÓÖŹĮæ¼õŠ”£¬µ±ĘųĢåĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»±äŹ±£¬·“Ó¦µ½“ļĘ½ŗāדĢ¬£¬¹ŹcÕżČ·£»d£®»ģŗĻĘųĢåµÄ×ÜÖŹĮæ²»±ä£¬ČŻĘ÷µÄČŻ»ż²»±ä£¬ĘųĢåĆܶȏ¼ÖÕ²»±ä£¬¹Źd“ķĪó£¬Õż·“Ó¦ŹĒĪüČČ·“Ó¦£¬ĘäĖūĢõ¼ž²»±ä£¬ĪĀ¶ČÉżøßĘ½ŗāÕżĻņŅĘ¶Æ£¬c(NO2)Ōö¼Ó£¬ŃÕÉ«¼ÓÉī£»
(2)¢ŁĻņ1LŗćČŻĆܱÕČŻĘ÷ÖŠĶ¶Čė1molCH4ŗĶ1molH2O(g)£¬·¢Éś·“Ó¦£ŗCH4(g)+H2OCO(g)+3H2(g)£¬·“Ó¦æŖŹ¼c(CH4)=1molL-1£¬¾¹żtmin£¬·“Ó¦“ļµ½Ę½ŗā£®ŅŃÖŖĘ½ŗāŹ±£¬c(CH4)=0.5molL-1£¬v(CH4)=![]() =
=![]() mol/(Lmin)£¬ĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬Ōņv(H2)=3v(CH4)=3”Į
mol/(Lmin)£¬ĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬Ōņv(H2)=3v(CH4)=3”Į![]() mol/(Lmin)=
mol/(Lmin)=![]() mol/(Lmin)£»
mol/(Lmin)£»
¢ŚT”ꏱ£¬1LŗćČŻĆܱÕČŻĘ÷ÖŠ
CH4(g)+H2O![]() CO(g)+3H2(g)
CO(g)+3H2(g)
ĘšŹ¼Įæ(mol)£ŗ 1 1 0 0
±ä»ÆĮæ(mol)£ŗ 0.5 0.5 0.5 1.5
Ę½ŗāĮæ(mol)£ŗ 0.5 0.5 0.5 1.5
Ę½ŗā³£ŹżK=![]() =
=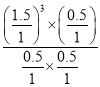 =6.75£»
=6.75£»
(3)ÓÉCO(g)ŗĶCH3OH(l)µÄČ¼ÉÕČČ”÷H·Ö±šĪŖ-283.0kJmol-1ŗĶ-725.8kJmol-1£¬Ōņ
¢ŁCO(g)+1/2O2(g)=CO2(g)”÷H=-283.0kJmol-1
¢ŚCH3OH(l)+3/2O2(g)=CO2(g)+2 H2O(l)”÷H=-725.8kJmol-1
¢ŪH2O(l)=H2O(g)”÷H=-44KJ/mol
ÓÉøĒĖ¹¶ØĀÉæÉÖŖÓĆ¢Ś-¢Ł+¢Ū”Į2µĆ·“Ó¦CH3OH(l)+O2(g)=CO(g)+2 H2O(g)£¬øĆ·“Ó¦µÄ·“Ó¦ČČ”÷H=-725.8kJmol-1-(-283.0kJmol-1)+2”Į44KJ/mol=-354.8kJmol-1£»
(4)¢ŁÓÉ300”ꏱ£¬Ōö“óŃ¹Ēæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬CH3OHµÄĢå»ż·ÖŹżŌö“ó£¬ĖłŅŌp1£¾p2£»
¢ŚÉčĻņĆܱÕČŻĘ÷³äČėĮĖ1molCOŗĶ2molH2£¬COµÄ×Ŗ»ÆĀŹĪŖx£¬Ōņ
CO(g)+2H2(g)ØTCH3OH(g)
ĘšŹ¼ 1 2 0
񄯒 x 2x x
½įŹų 1-x 2-2x x
ŌŚCµćŹ±£¬CH3OHµÄĢå»ż·ÖŹż=![]() =0.5£¬½āµĆx=0.75”£
=0.5£¬½āµĆx=0.75”£


 ±¦±“¼Ę»®ĘŚÄ©³å“Ģ¶į100·ÖĻµĮŠ“š°ø
±¦±“¼Ę»®ĘŚÄ©³å“Ģ¶į100·ÖĻµĮŠ“š°ø ÄÜæ¼ŹŌČ«ÄÜ100·ÖĻµĮŠ“š°ø
ÄÜæ¼ŹŌČ«ÄÜ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄ¬»ųĪŽŗ¦»Æ“¦ĄķŹ×ĻČŅŖĒó½«Ą¬»ų·ÖĄąŹÕ¼Æ”£Ä³¾ÓĆńŠ”ĒųĄ¬»ųŹÕ¼ÆµćÓŠČżøöĄ¬»ųĶ°£¬·Ö±š±źĆ÷”°³ųÓąĄ¬»ų”±”¢”°µē³Ų”±”¢”°æÉ»ŲŹÕĪļ”±”£ĻĀĮŠĪļÖŹÖŠ²»Ó¦Ķ¶Čė”°æÉ»ŲŹÕĪļ”±Ķ°ÄŚµÄŹĒ
A. ²£Į§Ėéʬ B. ĘĘĖÜĮĻŗŠ C. Ö½ÖĘ°ü×°ŗŠ D. ¹Ļʤ¹ūæĒ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·Ö×ÓÖŠĖłÓŠŌ×Ó²»æÉÄܶ¼ŌŚĶ¬Ņ»Ę½ĆęµÄĪļÖŹŹĒ
A. ŅŅČ² B. ŅŅĻ© C. ŅŅĶé D. ±½
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹Ų·“Ó¦»ņ¶ŌŹĀŹµ½āŹĶµÄĄė×Ó·½³ĢŹ½²»ÕżČ·µÄŹĒ
A£®Ź¢·ÅNaOHČÜŅŗµÄŹŌ¼ĮĘæ²»ÄÜÓĆ²£Į§Čū£ŗSiO2+2OH-=SiO32-+H2O
B£®Ė«ŃõĖ®ÖŠ¼ÓČėĻ”ĮņĖįŗĶKIČÜŅŗ£ŗH2O2+2H++2I-£½I2+2H2O
C£®ÓĆĶ×÷µē¼«µē½āCuSO4ČÜŅŗ£ŗ2Cu2++2H2O![]() 2Cu+O2”ü+4H+
2Cu+O2ӟ+4H+
D£®Ļū¶¾ŅŗÓė½ą²ŽĮé£ØÖ÷ŅŖ³É·ÖŹĒHCl£©»ģÓĆ£¬²śÉśÓŠ¶¾Cl2£ŗ2H++Cl-+ClO-£½Cl2+H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ2KMnO4+16HClØT2KCl+2MnCl2+5Cl2”ü+8H2O·“Ó¦ÖŠ
A. Ńõ»Æ²śĪļÓė»¹Ō²śĪļµÄĪļÖŹµÄĮæÖ®±ČĪŖ5£ŗ2
B. Ńõ»Æ²śĪļÓė»¹Ō²śĪļµÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ5
C. Ńõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ8
D. Ńõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ5£ŗ1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ĪļÖŹµÄĮæŹĒŅ»øöŠĀµÄĪļĄķĮ棬Ėü±ķŹ¾µÄŹĒĪļÖŹµÄÖŹĮæ
B£®ÖÜŅ»ÉĻĪēÉżĘģŅĒŹ½Ź±,ѧɜŗĶĄĻŹ¦µÄĪļÖŹµÄĮæ¹²ÓŠ2mol
C£®ĪļÖŹµÄĮæµÄµ„Ī»ŹĒĦ¶ū£¬¼ņ³ĘĦ£¬ÓĆmol±ķŹ¾
D£®Ė®µÄĦ¶ūÖŹĮæŹĒ18g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±£“ęÉŁĮ潚ŹōÄʵķ½·ØŹĒ£Ø””””£©
A.·ÅŌŚ×ŲÉ«ĘæÖŠ
B.·ÅŌŚCCl4ÖŠ
C.·ÅŌŚĖ®ÖŠ
D.·ÅŌŚĆŗÓĶÖŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij°ą»ÆѧŠĖȤŠ”×é×öČēĻĀŹµŃ飬ĒėÄć»Ų“šĻą¹ŲĪŹĢā£ŗ
¢ń”¢¼××éĶ¬Ń§ĻėÓĆ½šŹōÄĘŗĶæÕĘųÖʱø“æ¶Č½ĻøßµÄNa2O2(²»æ¼ĀĒæÕĘųÖŠN2)£¬æÉĄūÓƵÄ×°ÖĆČēĻĀ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
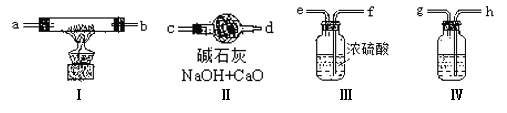
(1)×°ÖĆ¢ōÖŠŹ¢·ÅµÄŅ©Ę·ŹĒ £¬ČōƻӊøĆ×°ÖĆæÉÄܵ¼ÖĀÉś³ÉµÄNa2O2ÖŠŗ¬ÓŠ £¬Ęä·“Ó¦·½³ĢŹ½ĪŖ ”£
(2)Čō¹ę¶ØĘųĢåµÄĘųĮ÷·½Ļņ“Ó×óµ½ÓŅ£¬ø÷ŅĒĘ÷½ÓæŚµÄ±źŗÅ×ÖÄø(a”¢b””)Ė³ŠņŹĒ£ŗ
æÕĘų½ųČė £¬ ½Ó £¬ ½Ó £¬ ½Ó ”£
(3)×°ÖĆµÄ¢ņ×÷ÓĆŹĒ ”£
¢ņ”¢ŅŅ×éĄūÓĆĻĀĶ¼ĖłŹ¾ŹµŃé×°ÖĆ½ųŠŠÄ³Š©ĘųĢåµÄÖʱø”¢ŠŌÖŹµČŹŌŃé(Ķ¼ÖŠ¼Š³Ö×°ÖĆÓŠŹ”ĀŌ)”£
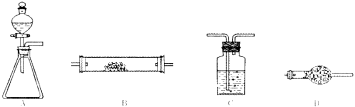
(4)ĪŖŃéÖ¤ĀČĘų²»ÄÜŹ¹øÉŌļµÄŗģ²¼ĢõĶŹÉ«£¬ÖĆŗģ²¼ĢõÓŚBÖŠ£¬°“A-C-B-DĮ¬½Ó³ÉŹµŃé×°ÖĆĢåĻµ”£A׶ŠĪĘæÖŠŹŌ¼ĮŃ”ÓĆøßĆĢĖį¼Ų¾§Ģ壬Ōņ·ÖŅŗĀ©¶·ÖŠµÄŅŗĢåŹĒ £»AÖŠ·¢ÉśµÄ»Æѧ·½³ĢŹ½ŹĒ £¬CÖŠŹŌ¼ĮŹĒ £¬DµÄ×÷ÓĆŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”¢B”¢C”¢D”¢E”¢WĪŖĮłÖÖĒ°ĖÄÖÜĘŚŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£® A Óė D Ķ¬Ö÷×壬æÉŠĪ³É DA ŠĶĄė×Ó»ÆŗĻĪļ£¬BÓėCĶ¬ÖÜĘŚĒŅĻąĮŚ£¬CÓėEĶ¬Ö÷×壬E2-Óė Ar Ō×Ó¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£¬W µÄŗĻ½šÓĆĮæ×ī“ó”¢ÓĆĶ¾×ī¹ć£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)D ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆ___________£®
(2)A ·Ö±šÓė C”¢E ŠĪ³É×ī¼ņµ„»ÆŗĻĪļÖŠ·Šµć½ĻøߵďĒ________(Ģī»ÆѧŹ½)£¬ŌŅņŹĒ____________£®
(3)A”¢C”¢DČżÖÖŌŖĖŲŠĪ³ÉµÄĪļÖŹÖŠŗ¬ÓŠµÄ»Æѧ¼üĄąŠĶ______£¬×ĘČȵÄĢ¼ÄÜÓė B µÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄÅØČÜŅŗ·“Ó¦£¬»Æѧ·“Ó¦·½³ĢŹ½ĪŖ_____________£®
(4)ĻņŹ¢ÓŠA2C2 ČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČė¼øµĪĖį»ÆµÄWEC4 ČÜŅŗ£¬ČÜŅŗ±ä³É×Ų»ĘÉ«£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ____________£»Ņ»¶ĪŹ±¼äŗó£¬ČÜŅŗÖŠÓŠĘųÅŻ³öĻÖ£¬²¢·ÅČČ£¬ĖęŗóÓŠŗģŗÖÉ«³ĮµķÉś³É£¬²śÉśĘųÅŻµÄŌŅņŹĒ_______£»Éś³É³ĮµķµÄŌŅņŹĒ____________(ÓĆĘ½ŗāŅʶÆŌĄķ½āŹĶ)£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com