
某短周期元素R,它的最高价氧化物中含氧为60%,它的氢化物中含R为94.12%.R元素原子核内质子数和中子数相等.通过计算求R元素的相对原子质量,并指出它在周期表中的位置.(已知氧元素的相对原子质量为16)
考点: 原子结构与元素的性质.
专题: 元素周期律与元素周期表专题.
分析: 设R的相对原子质量为M,最外层电子数为x,则其最高正价为+x,负极为﹣(8﹣x),所以它的氢化物的化学式为 H8﹣xR,最高价氧化物的化学式为R2Ox;根据已知数据计算M,再根据质子数和中子数相等,计算质子数,然后判断元素.
解答: 解:设R的相对原子质量为M,最外层电子数为x,则其最高正价为+x,负极为﹣(8﹣x),
所以它的氢化物的化学式为 H8﹣xR,最高价氧化物的化学式为R2Ox;
根据已知数据计算M,再根据质子数和中子数相等,计算质子数,然后判断元素.
它的最高价氧化物中含氧为60%,氢化物中含R为94.12%
则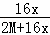 =60%,
=60%,
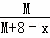 =94.12%,
=94.12%,
解得M=32,x=6,
所以R的相对原子质量为32,R中质子数和中子数相等,则其质子数为16,即为S元素,在第三周期第VIA族;
答:R的相对原子质量为32,该元素位于第三周期第VIA族.
点评: 本题考查了元素的推断,题目难度不大,注意把握元素最高正价与负极之间的关系,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:
在Na+浓度为0.5mol•L﹣1的某澄清溶液中,还可能含有下表中的若干种离子.
阳离子 K+Ag+Mg2+Ba2+
阴离子 NO3﹣、CO32﹣、SiO32﹣、SO42﹣
现取该溶液100mL进行如下实验(气体体积均在标准状况下测定).
序号 实验内容 实验结果
Ⅰ 向该溶液中加入足量稀盐酸 产生白色沉淀并放出标准状况下0.56L气体
Ⅱ 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 固体质量为2.4g
Ⅲ 向Ⅱ的滤液中滴加BaCl2溶液 无明显现象
请回答下列问题.
(1)实验Ⅱ,混合液过滤后如何洗涤沉淀? .
(2)澄清溶液中一定不存在的离子是 .
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写表中阴离子的物质的量浓度(能计算出结果的填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
阴离子 NO3﹣ CO32﹣ SiO32﹣ SO42﹣
c/mol•L﹣1 ?
(4)判断K+是否存在,若存在,求其最小浓度,若不存在,请说明理由: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列结果是马虎同学回答同桌提问的答案,你认为需要改正的是()
①微粒半径:S2﹣>Cl﹣>S>Cl ②氢化物稳定性:HF>HCl>H2S>PH3③还原性:Na>Mg>Al>K ④氧化性:Cl2>S>O2>F2 ⑤酸性:H2SO4>HClO4>H2SiO3>H3PO4 ⑥得电子能力:F>Cl>Br>I.
A. 只有③ B. ③④⑤ C. ②④⑤⑥ D. ③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中错误的是()
A. 在由氢氧化铜分解制氧化铜时,要边加热边用玻璃棒搅拌
B. 用药匙或者纸槽把粉末状药品送入试管的底部
C. 过滤时玻璃棒的末端应轻轻靠在三层的滤纸上
D. 如果没有试管夹,可以临时手持试管给固体或液体加热
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿伏加德罗常数,下列说法正确的是()
A. 1mol Na2O2与水反应时,转移电子的数目为2NA
B. 标准状况下,22.4L水中含有水分子的数目为NA
C. 14g N2中含有电子的数目为7NA
D. 数目为NA的一氧化碳分子和0.5mol甲烷的质量比为7:4
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现血红色.
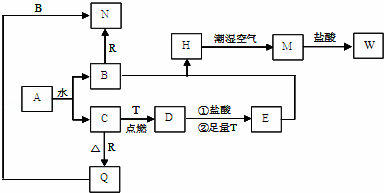
(1)写出下列物质的化学式:D: E: N: .
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象: ;
(3)按要求写方程式:
B和R反应生成N的离子方程式: ;
M→W的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是(NA表示阿伏加德罗常数)()
A. 常温常压下,22.0 gCO2所含的电子数为22NA
B. 常温常压下,1mol氦气含有原子数为NA
C. 0.5mol•L﹣1 Na2CO3溶液中含有Na+离子的数目为NA
D. 标准状况下,22.4LCCl4含有的氯原子数为4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com