
| A����a=b�����Ϻ���Һ��pH��7 |
| B������Ϻ���ҺpH=7����c��M+����c��Cl-�� |
| C����a=2b����c��M+����c��Cl-����c��MOH����c��OH-����c��H+�� |
| D������Ϻ���Һ����c��H+��=c��OH-��+c��MOH��������Ƴ�a=b |


 ��У���˿��ֿ���ϵ�д�
��У���˿��ֿ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
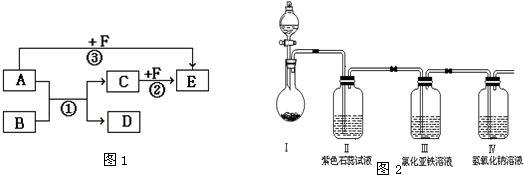
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Fe | B��H | C��I | D��F |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ʹpH��ֽ�����ɫ����Һ�У�Fe3+��Cl-��Ba2+��Br-�ܴ������� | ||||
B�����Ե缫����Ȼ�����Һ��2Cl-+2H2O
| ||||
| C��þ�뼫ϡ���ᷴӦ��������淋����ӷ���ʽΪ��4Mg+6H++NO3-=4Mg2++NH4++3H2O | ||||
| D����10 mL 0.1 mol?L-1 KAl��SO4��2��Һ��10 mL 0.2 mol?L-1Ba��OH��2��Һ��ϣ��õ��ij�����Al��OH��3��BaSO4�����ʵ���֮��Ϊ1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ȵ�ͭ˿�����������ȼ�գ������ػ�ɫ���� |
| B������������ȼ�գ����ɰ�ɫ���� |
| C��������H2��Cl2�а�����ȼ�գ�������ɫ���棬����ƿ�ڳ��ְ�ɫ���� |
| D����������ˮ��Ӧ���ɴ���������ᣬ������ˮ���ձ�Ϊϡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ۢ� | B���ڢۢܢ� |
| C���ڢݢޢ� | D���ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����������ϩ��
����������ϩ�� ���ͱ����⻯�����ݣ�������˵����ȷ���ǣ�������
���ͱ����⻯�����ݣ�������˵����ȷ���ǣ�������| ������ |  +H2 +H2 |  +2H2 +2H2 | 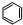 +3H2 +3H2 |
| �⻯�ȡ�H ��kJ?mol-1�� | -119.7 | -232.7 | -208.4 |
| A��������ϩ��H2�ķ�Ӧ����� |
B�����������£�1 mol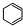 ת��Ϊ ת��Ϊ ʱ����113kJ ʱ����113kJ |
| C������ϩ��������ϩ�ͱ�����ͬ�Ĺ����� |
| D�����ֻ������л�����ϩ���ȶ�����ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A���������Ľṹ��ʽ��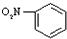 |
| B�������ǵ�ʵ��ʽ�����ʽ��Ϊ��C6H12O6 |
C������ķ��ӱ���ģ��ͼΪ�� |
D��CH3Cl�ĵ���ʽ��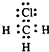 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com