
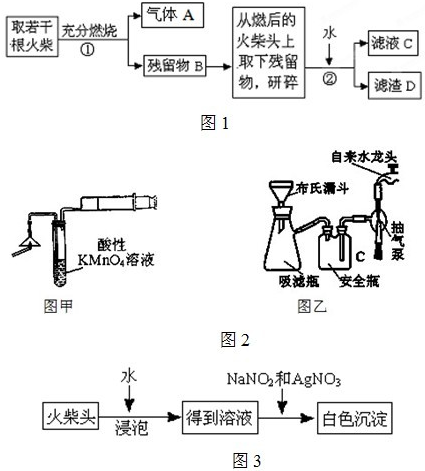
某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S,设计了以下实验流程图:
|
|
(1)为验证气体A,按右图所示进行实验:若能
观察到 的现象,即可证明火柴头上
含有S元素。
(2)步骤②的实验操作装置如右图所示,该操
作的名称是 ,其工作原理是 。
(3)要证明火柴头中含有Cl元素的后续实验步
骤是 。
(4)有学生提出检验火柴头上KClO3另一套实验
方案:
|
|
提出上述方法中出现白色沉淀并不能充分说明火
柴头上KClO3的存在,其理由是 。
(5)该小组猜测滤渣D对双氧水分解制氧气的速率会产生一定的影响,设计并进行了以下5次实验。
| 实验次数 | H2O2溶液质量分数% | H2O2溶液用量/毫升 | 物质D用量/克 | 反应温度/℃ | 收集气体体积/毫升 | 所需时间/秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 30 | 5 | 0 | 55 | 2 | 10.5 |
由上表可知,实验①和⑤能证明温度越高,化学反应速率越快,实验 和 证明物质D的用量越大,反应速率越快。
(6)写出步骤①中发生反应的化学方程式 。
(1)KMnO4溶液(紫红色)褪色
(2)减压过滤(或抽滤), 工作原理是:当找开自来水龙头,装置内部的空气随自来水被带走,导致装置内部压强减小,使过滤速度加快,得到较干燥的固体物质。
(3)取滤液C,加入HNO3和AgNO3溶液,若观察到白色沉淀产生,即可证明火柴头中含有氯元素。
(4)ClO3??+3NO2??+Ag+=AgCl↓+3NO3??
AgNO2与AgCl均为不溶于水的白色沉淀。
(5)②和③
![]() (6)2KClO3
(6)2KClO3![]() 2KCl+3O2↑ S+O2
2KCl+3O2↑ S+O2![]() SO2
SO2
⑴若火柴头中含有S,则会燃烧生成SO2,通入酸性KMnO4溶液可以发生氧化还原反应使其褪色;
⑵操作②用的是减压过滤(或抽滤),工作原理是:当找开自来水龙头,装置内部的空气随自来水被带走,导致装置内部压强减小,使过滤速度加快,得到较干燥的固体物质。
⑶2KClO3受热分解生成KCl,再加入HNO3和AgNO3溶液,若观察到白色沉淀产生,即可证明火柴头中含有氯元素。
⑷有关的离子反应方程式为ClO3??+3NO2??+Ag+=AgCl↓+3NO3??;AgNO2与AgCl均为不溶于水的白色沉淀。
⑸对比实验中,必须保持所要改变条件以外的其他条件不能改变,所以除D的量变化外,其他条件不能改变。故为②的③。
![]() ⑹步骤①中发生反应的化学方程式为2KClO3
⑹步骤①中发生反应的化学方程式为2KClO3![]() 2KCl+3O2↑ S+O2
2KCl+3O2↑ S+O2![]() SO2
SO2


科目:高中化学 来源: 题型:阅读理解

| ||
| △ |
| ||
| ||
| △ |
| ||

| 实验序号 | H2O2溶液 质量分数% |
H2O2溶液 用量/毫升 |
物质D用量(g) | 反应温度(℃) | 收集气体 体积/毫升 |
所需时间(秒) |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 30 | 5 | 0 | 55 | 2 | 10.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验次数 | H2O2溶液质量分数% | H2O2溶液用量/毫升 | 物质D用量/克 | 反应温度/℃ | 收集气体体积/毫升 | 所需时间/秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 30 | 5 | 0 | 55 | 2 | 10.5 |
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| △ |
| ||
| ||
| △ |
| ||


查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 实验次数 | H2O2溶液质量分数% | H2O2溶液用量/毫升 | 物质D用量/克 | 反应温度/℃ | 收集气体体积/毫升 | 所需时间/秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 30 | 5 | 0 | 55 | 2 | 10.5 |
| ||
| △ |
| ||
| ||
| △ |
| ||
查看答案和解析>>
科目:高中化学 来源:2010年浙江江山实验中学高二年级5月月考化学试卷 题型:实验题
火柴是人们常用的生活用品,某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S等物质,设计了以下系列实验,并回答下列各题。
Ⅰ、火柴头中硫元素的实验证明
A B
⑴设计装置A中可观察到 的实验现象,即可证明火柴头上含有S元素。
⑵甲同学认为B装置中除了可选用稀高锰酸钾外还可选用:品红溶液、紫色石蕊溶液、滴有酚酞的NaOH溶液、溴水等,经大家分析后淘汰了紫色石蕊溶液和滴有酚酞的NaOH 溶液。你认为淘汰的原因可能是 。甲同学还认为在A装置中选用浓的高锰酸钾酸性溶液更好,因为浓度越大反应速率越快,你认为对吗? (先判断再说明原因)。
Ⅱ、火柴头中含有Cl元素的证明,设计了以下实验流程图:
⑴为验证火柴头中含有Cl元素的实验步骤是:取滤液C……请回答后续实验步骤 是 。
⑵有学生提出检验火柴头上KClO3另一套实验方案:
|
|

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com