
| A. | 105g | B. | 106.1g | C. | 107.6g | D. | 108.3g |
分析 根据质量守恒定律、“9.4gCaCO3和K2CO3的固体混合物,测得其中含有氧元素的质量为3.6g”,可以计算出碳酸根的质量,从而计算二氧化碳的质量,进而求出所得不饱和溶液的质量.
解答 解:根据质量守恒定律、“9.4gCaCO3和K2CO3的固体混合物,测得其中含有氧元素的质量为3.6g”,则可以计算出碳酸根的质量为:3.6g÷($\frac{16×3}{12+16×3}$×100%)=4.5g,而碳酸根离子与稀盐酸反应生成二氧化碳和水,则设生成二氧化碳的质量为x.
CO32-~CO2
60 44
4.5g x
则$\frac{60}{44}=\frac{4.5g}{x}$,解得x=3.3g.
故最后所得不饱和溶液的质量9.4g+100g-3.3g=106.1g.
故选B.
点评 此题是一道化学计算题,解题的关键是质量守恒定律的巧妙使用,此题难度较大,是一道综合性较强的计算题.


科目:高中化学 来源: 题型:选择题
| A. | 蛋白质溶液遇CuSO4后产生的沉淀能重新溶解 | |
| B. | 淀粉水解的最终产物是葡萄糖 | |
| C. | 葡萄糖能发生氧化反应和水解反应 | |
| D. | 植物油不能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2O2中阴阳离子的个数比为1:1 | |
| B. | Na2O2投入到酚酞溶液中,溶液变红 | |
| C. | Na2O2投与FeCl2溶液的反应:能将Fe2+氧化成Fe3+,得到Fe(OH)3沉淀 | |
| D. | Na2O2与水反应,Na2O2既是氧化剂,又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,当剩余少量水时用余热蒸干 | |
| B. | 蒸馏操作时,应使温度计水银球与蒸馏烧瓶的支管口相平 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 3:1:1 | C. | 1:3:3 | D. | 6:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
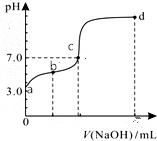 常温下向20mL0.1mol/LHA溶液中逐滴加入0.1mol/LNaOH溶液,其pH变化情况如图所示(忽略温度变化).下列说法中不正确的是( )
常温下向20mL0.1mol/LHA溶液中逐滴加入0.1mol/LNaOH溶液,其pH变化情况如图所示(忽略温度变化).下列说法中不正确的是( )| A. | 由题可知HA为弱酸 | |
| B. | 滴定终点位于c和d点之间 | |
| C. | 滴定到b点时:n(Na+)+n(H+)-n(OH-)+n(HA)=0.002mol | |
| D. | 滴定到d点时:c(OH-)>c(Na+)>c(A-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
已知HNO2在低温下较稳定,酸性比醋酸略强,既有氧化性又有还原性,其氧化产物、还原产物与溶液pH的关系如下表。下列有关说法错误的是
pH范围 | >7 | <7 |
产物 | NO3- | NO、N2O、N2中 |
A.碱性条件下,NaNO2与NaClO反应的离子方程式为NO2-+ClO-=NO3-+Cl-
B.向冷的NaNO2溶液中加入滴有淀粉的氢碘酸,溶液变蓝色
C.向冷的NaNO2溶液中加入稀硫酸可得到HNO2
D.向冷的NaNO2溶液中通入CO2可得到HNO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com