
| A. | △H1>△H2>△H3 | B. | △H1<△H3<△H2 | C. | △H1=△H3>△H2 | D. | △H2=△H3<△H1 |
分析 25℃,101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ/mol,注意弱电解质的电离吸热,由此来解答.
解答 解:强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O,△H=-57.3kJ/mol,向1L1mol•L-1的下列溶液中分别加入1L1mol•L-1的NaOH溶液中加入:①稀醋酸;②稀硫酸;③稀盐酸,醋酸溶于水吸热,则放出的热量最低,焓变最大,稀硫酸和稀盐酸都是强的稀酸,所以氢氧化钠的量一定的条件下,二者放出的热量相等,即放出的热量为△H2=△H3<△H1,
故选:D.
点评 本题主要考查了中和热大小的比较,需要注意的是弱电解质的电离吸热,浓硫酸溶于水放热以及比较大小时要考虑“-”号.


科目:高中化学 来源: 题型:推断题
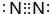 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Ni(OH)2 |
| 开始沉淀的pH | 1.1 | 6.5 | 3.5 | 7.1 |
| 沉淀完全的pH | 3.2 | 9.7 | 4.7 | 9.2 |
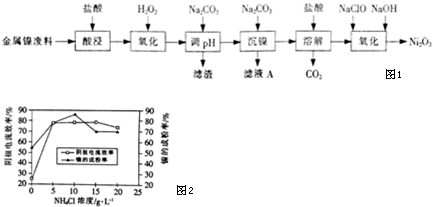
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
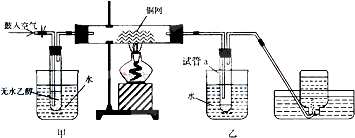
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al是该电池的正极 | B. | H2O2在石墨电极上发生氧化反应 | ||
| C. | 石墨电极附近溶液的pH增大 | D. | 海水中的Cl-向正极移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com