
| A. | 该溶液中:2c (H+)=c(A-)+c(OH-) | |
| B. | 由pH=3的HA溶液与pH=11的NaOH溶液等体积混合,所得溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) | |
| C. | 浓度均为0.1 mol•L-1的HA和NaA溶液等体积混合,所得溶液中:c(A-)>c(HA)>c(Na+)>c(OH-)>c(H+) | |
| D. | 0.1 mol•L-1 HA溶液与0.05 mol•L-1 NaOH溶液等体积混合,所得溶液中:2c(H+)+c(HA)═c(A-)+2c(OH-) |
分析 常温下,0.1mol•Ll-1某一元酸(HA)溶液的pH=3,说明该酸在其水溶液里只有部分电离,所以是弱酸.
A.根据电荷守恒定律分析;
B.pH=3的HA溶液与pH=11的NaOH溶液等体积混合,酸有剩余;
C.应比较酸的电离程度和酸根离子的水解程度的相对大小;
D.混合溶液中存在浓度均为0.025 mol•L-l的HA和NaA溶液,根据电子守恒和物料守恒式综合判断.
解答 解:常温下,0.1mol•Ll-1某一元酸(HA)溶液的pH=3,说明该酸在其水溶液里只有部分电离,所以是弱酸,
A.根据电荷守恒得c(H+)=c(A-)+c(0H-),故A错误;
B.pH=3的HA与pH=11的Na0H溶液中,酸的浓度大于碱的浓度,等体积混合时酸的物质的量大于碱,所以酸和碱反应后酸有剩余,溶液中c(A-)>c(Na+),故B错误;
C.浓度均为0.1 mol•L-l的HA和NaA溶液等体积混合,若酸的电离程度大于酸根离子的水解程度,所以所得溶液中:c(Na+)>c(HA),故C错误;
D.混合溶液中存在浓度均为0.025 mol•L-l的HA和NaA溶液,根据电荷守恒得c(H+)+c(Na+)=c(OH-)+c(A-),根据物料守恒得:2c(Na+)=c(A-)+c(HA),根据质子守恒得c(OH-)=c(H+)+c(HA),所以2c(H+)+c(HA)=c(A-)+2c(OH-),故D正确;
故选D.
点评 本题考查酸碱混合溶液中离子浓度大小的比较,根据电荷守恒、物料守恒及质子守恒来分析解答,难度较大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | SO2具有漂白性,用SO2漂白过的草帽辫能长久持白 | |
| B. | SiO2、CO2都是酸性氧化物,都能与强碱溶液反应 | |
| C. | NO2为红棕色气体,因此,将NO2通入水中,溶液显红棕色 | |
| D. | 漂白粉的有效成分是CaCl2和Ca(ClO)2,应密封保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 残留固体中一定不含有铁 | B. | 滤液中可能含有Fe3+ | ||
| C. | 原混合物中n(Fe)>n(Fe2O3)+n(CuO) | D. | 原混合物中铁为3.36 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
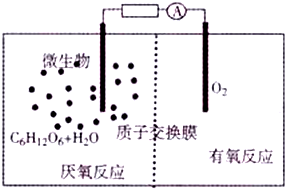 微生物电池是指在微生物的作用下将化学能转化为电能的装置(总反应方程式为C6H12O6+6O2═6CO2+6H2O),其工作原理如图所示.下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置(总反应方程式为C6H12O6+6O2═6CO2+6H2O),其工作原理如图所示.下列有关微生物电池的说法错误的是( )| A. | 正极区溶液的pH减小 | |
| B. | 微生物促进了反应中电子的转移 | |
| C. | 质子通过交换膜从负极区移向正极区6H2O+C6H12O6-24e-═6CO2+24H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cd(OH)2 | B. | Cd(OH)2 | C. | Cd | D. | NiO(OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2溶于水生成的H2SiO3的酸性弱于H2CO3 | |
| B. | SiO2是一种空间立体网状结构的晶体,熔点高、硬度大 | |
| C. | 在SiO2晶体中,每个硅原子周围结合2个氧原子 | |
| D. | SiO2是一种酸性氧化物,所以不和任何酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸与氢氧化钡溶液 | B. | 稀硫酸与氢氧化钡溶液 | ||
| C. | 稀硫酸与稀氨水 | D. | 盐酸与氢氧化铁胶体反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
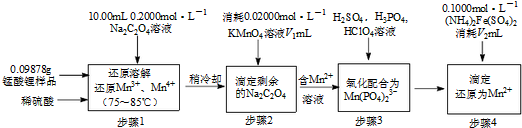
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+、Al 3+、Fe3+、Cu2+、Ba2+ |
阴离子 | OH-、Cl-、CO32-、NO3-、SO4- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com