
G��һ���������ϵ���Ҫ�ɷ�֮һ����ṹ�к���������Ԫ����G�ĺϳ�·������(���ֲ���Ͳ��ַ�Ӧ������ȥ)��


��֪��
��B�к˴Ź�������ͼ��ʾ��������6�ֲ�ͬ��������ԭ�ӣ�
��D��F��Ϊͬϵ�
��ش��������⣺
��1��(CH3)2C��CH2��ϵͳ����������Ϊ ������B��һ���ķ�Ӧ����Ϊ ��
��2��E�Ľṹ��ʽΪ ��F�����к��еĺ��������������� ��
��3��C��������ɵõ�һ����������������Һ����������Ӧ�����ʣ���д����������Ӧ�Ļ�ѧ����ʽ ��
��4��F����һ�������ºϳɸ߷��ӻ������д���ø߷��ӻ�����Ľṹ��ʽ ��
��5��ͬʱ������������������FeCl3��Һ������ɫ��Ӧ���ڱ�����������ȡ������������̼��������Һ��Ӧ�ų����壻������D��ͬ���칹�干�� ��(�����������칹)��
��6������պϳ�·���б���ϩ�ϳ�F�ķ�����д����1-��ϩ��ȡ2-�ǻ����� �ĺϳ���·�� ��
�ĺϳ���·�� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ��ͷ�и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ���¶��£����淴ӦA(g) �� 3B(g) 2C(g)�ﵽƽ��ı�־��
2C(g)�ﵽƽ��ı�־��
A�������ڵ�ѹǿ����ʱ��仯
B��A��B��C��Ũ�Ȳ��ٱ仯
C����λʱ��������n mol A��ͬʱ����2n mol C
D��A��B��C�ķ�����֮��Ϊ1�U3�U2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ��ɽ�и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���̴���������������������ʣ�����ʽΪC27H46O�����̴���һ��������Һ�����ϣ������ʽΪC34H50O2����ϳ����ֵ��̴���������
A��C6H13COOH B��C6H5COOH C��C7H15COOH D��C6H5CH2COOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ܴ������棬���Ҽ���AL���ܲ����������ǣ� ��
A��H+,Mg2+,Al3+,CO32-
B��Na+,Al3+,Cl-,Ba2+
C��OH-,Al3+,Cl-,NO3-
D��OH-,Ba2+,Cl-,NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�У����������ֻ�����Ӧ���ͣ�������������ԭ��Ӧ���ǣ� ��
A��2Na + 2H2O = 2NaOH + H2��
B��CH4 + 2O2 CO2 +2H2O
CO2 +2H2O
C��2KClO3 2KCl + 3O2��
2KCl + 3O2��
D��CaCO3+2HCl = CaCl2+H2O+CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ����ʮУ���н̸Ĺ�ͬ��߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
ȫ��Һ�������һ�����͵���ɫ�������ܵ�ء������ܷ�ӦΪ��V3++VO2++H2O  VO2++2H++V2+������˵����ȷ����
VO2++2H++V2+������˵����ȷ����
A���ŵ�ʱ������ӦΪ��VO2++2H++e-=VO2++H2O
B�����ʱ������ӦΪ��V2+-e-=V3+
C���ŵ�����е����ɸ��������·���������������������������Һ����
D���������У�H+����������������Ǩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ����ʮУ���н̸Ĺ�ͬ��߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ������������ȷ����
A����0.1 mol NaHSO4������������������������Ϊ0.3NA
B��25��ʱ��pH=13��1.0 LBa(0H)2��Һ�к��е�OH����ĿΪ0.2NA
C�����³�ѹ�£�4.4gCO2��N2O������������е�ԭ����Ϊ0.3 NA
D��1L1 mol��L��1FeCl3��ȫˮ������NA����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ������һ�и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��Һ�п��ܺ���H+��Na+��NH4+��Mg2+��Fe3+��Al3+��SO42-��HCO3�������ӡ��������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ���������ɳ������ʵ�����NaOH��Һ������仯��ͼ��ʾ������˵����ȷ���� �� ��
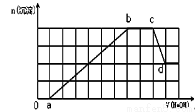
A��ab�η��������ӷ�ӦΪ��Al3++3OH��= Al��OH��3���� Mg2++2OH��= Mg��OH��2��
B��ԭ��Һ�к��е������ӱض���H+��NH4+��Al3+��Mg2+
C��ԭ��Һ�к��е�Fe3+��Al3+�����ʵ���֮��Ϊ1:1
D��d����Һ�к��е�����ֻ��NaAlO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ʵ����
��ҵ����ij����������Cu2O��Al2O3��Fe2O3��SiO2����ȡͭ�IJ�����������:
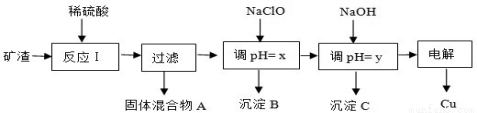
��֪�� Cu2O + 2H+ = Cu + Cu2+ + H2O
������ | Cu��OH��2 | Al��OH��3 | Fe��OH��3 | Fe��OH��2 |
��ʼ����pH | 5.4 | 4.0 | 1.1 | 5.8 |
������ȫpH | 6.7 | 5.2 | 3.2 | 8.8 |
��1����������A�еijɷ��� ��
��2����Ӧ����ɺ���Ԫ�صĴ�����ʽΪ ���������ӷ��ţ���д�����ɸ����ӵ����ӷ���ʽ ��
��3��x��y��Ӧ����ֵ��Χ�ֱ��� �� ��
��4����ⷨ��ȡCuʱ��������ӦʽΪ ��������ӦʽΪ ��
��5�����й���NaClO��pH��˵����ȷ���� ��
a. ����NaClO��ʹ��Һ��pH����
b. NaClO�ܵ���pH����Ҫԭ�������ڷ�����ӦClO��+ H+ HClO�� ClO������H+���Ӷ��ﵽ����pH��Ŀ��
HClO�� ClO������H+���Ӷ��ﵽ����pH��Ŀ��
c .NaClO�ܵ���pH����Ҫԭ��������NaClOˮ��ClO��+ H2O HClO+OH����OH������H+ ���Ӷ��ﵽ����pH��Ŀ��
HClO+OH����OH������H+ ���Ӷ��ﵽ����pH��Ŀ��
��6����NaClO��pH�����ɳ���B��ͬʱ����һ�־���Ư�����õ����ʣ��÷�Ӧ�����ӷ���ʽΪ_________________________ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com