
����Ŀ��һ�������£���3molA��1molB�����������ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A(g)+B(g) ![]() xC(g)+2D(s)��2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.2mol/L�������ж���ȷ����
xC(g)+2D(s)��2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.2mol/L�������ж���ȷ����
A���ӿ�ʼ��ƽ��A��ƽ����Ӧ����Ϊ0.3mol/(L![]() s)
s)
B���ӿ�ʼ��ƽ��B��ת����Ϊ60%
C���˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ![]()
D�������������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬
���𰸡�D
��������
���������һ�������£���3molA��1molB�����������ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A(g)+B(g)![]() xC(g)+2D(s)��2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.2mol/L�����ݻ�ѧƽ������ʽ��ʽ���㣻
xC(g)+2D(s)��2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.2mol/L�����ݻ�ѧƽ������ʽ��ʽ���㣻
3A(g)+B(g)![]() xC(g)+2D(s)
xC(g)+2D(s)
��ʼ��(mol) 3 1 0 0
�仯��(mol) 1.2 0.4 0.4x 0.8
ƽ����(mol) 1.8 0.6 0.4x 0.8
C��Ũ��Ϊ0.2mol/L��C�����ʵ���Ϊ0.4������õ�x=1��A��A��ƽ����Ӧ����=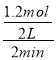 =0.3mol/(Lmin)����A����B��B��ת����=
=0.3mol/(Lmin)����A����B��B��ת����=![]() ��100%=40%����B����C��DΪ���壬�������´˷�Ӧ�Ļ�ѧƽ�ⳣ��=
��100%=40%����B����C��DΪ���壬�������´˷�Ӧ�Ļ�ѧƽ�ⳣ��=![]() ����C����D����Ӧ�������к��й��壬�ܶȵ�����������������������������������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬����D��ȷ����ѡD��
����C����D����Ӧ�������к��й��壬�ܶȵ�����������������������������������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬����D��ȷ����ѡD��


 ���ɿ��õ�Ԫ����AB��ϵ�д�
���ɿ��õ�Ԫ����AB��ϵ�д� С�����ϵ�д�
С�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧ-ѡ��5���л���ѧ������
GΪ�ϳɿ�������ҩ���м��壬F�ܷ���������Ӧ���ϳ�G��·�����£�
��֪��
��1����A������Ϊ_______________��G�еĹ�����������_____________��
��2��D��E�Ļ�ѧ��Ӧ����ʽΪ____________________��F�Ľṹ��ʽΪ__________________��
��3������B�й����ŵ��Լ�Ϊ___________��
��4�������³�������G��ͬ���칹����__________�֡�
�����Ȼ����ܷ�����ɫ��Ӧ ��������һ�ȴ���ֻ��һ�� ���˴Ź�������ֻ���������շ�
��5����G�ϳɿ�������ҩ��L�ĺϳ�·�����£�
H�Ľṹ��ʽΪ___________����д��K�Ľṹ��ʽ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F���ֶ���������Ԫ�أ�A�ļ�������ɫ��ӦΪ��ɫ��B������������Ӧˮ����B(OH)2 5.8 gǡ������100 mL 2 mol��L-1������ȫ��Ӧ����Bԭ�Ӻ�������������������ȡ�E2�ڻ���ɫ����C2��ȼ�ղ�����ɫ���档Dԭ�ӵ������������Ǵ�����������3����F��Dͬ���塣 �������������ش�
��1��д��Ԫ��B������ ��Ԫ��C��Ԫ�����ڱ��е�λ�� ��
��2��A��D�γɵ���ɫ������������к��еĻ�ѧ������Ϊ ��
��3��C2��ADE��Һ��Ӧ�����ӷ���ʽΪ ��
��4���õ���ʽ��ʾBC2���γɹ��� ��
��5����Ԫ��D��E���ɵ�9e���������� ��
��6���Ƚ�Ԫ��C��F����̬�⻯����ȶ��� �� ���û�ѧʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦH2��g��+ I2��g��![]() 2HI��g����1 mol H2��ȫ��Ӧ�ų�a kJ�������������±����ݣ�����˵������������ ��
2HI��g����1 mol H2��ȫ��Ӧ�ų�a kJ�������������±����ݣ�����˵������������ ��
�� ѧ �� | H��H | I��I |
�Ͽ�1 mol��ѧ��ʱ���յ�������kJ�� | b | c |
A���÷�Ӧ�з�Ӧ��������������������������
B���Ͽ�1 mol H-H ����1 mol I-I �������������ڶϿ�2 mol H-I ����������
C���Ͽ�2 mol H-I����������Ϊ��a+b+c��kJ
D�����ܱ������м���2 mol H2��2 mol I2����ַ�Ӧ��ų�������С��2a kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ����2 L�ܱ������У�������̬����X��Y��Z�����ʵ�����n����ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ����ɵã�
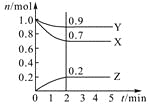
��1���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��2����Ӧ��ʼ��2 min����Y��ʾ��ƽ����Ӧ����Ϊ ��X��ת����Ϊ ��
��3����һ���¶��£������������Ϊ������Ӧ�ﵽ��Ӧ�ȵı�־���� ��
A��X��Y��Z��Ũ����� |
B��X��Y��Z�ķ�������Ϊ3�U1�U2 |
C��Z������������Y���������ʵĶ��� |
D����λʱ��������n mol Y��ͬʱ����3n mol X |
��4�����ܱ������ͨ��a mol A��g����b mol B��g����
������ӦA��g��+ B��g��= 2C��g�������ı���������ʱ����ӿ췴Ӧ���ʵ��� ������ţ���
�������¶�
������������������䣬���뺤��
���������
������������������䣬����A��g�������ʵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�������Դ�Ͳ��ϵ������У��������
A�����ά���Զ�������Ϊ��Ҫԭ���Ƴɵ�
B�����������غ������˽���������վ�������Դ��ȱ����
C�����ࡢ��֬�������ʶ�������Ȼ�л��߷��ӻ�����
D���������߱���ˢ��������ڸ��ﴦ���棬������Ч����������ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ƚ����и����Ȼ�ѧ����ʽ�Ц�H�Ĵ�С��ϵ��
(1)S(s)��O2(g)===SO2(g) ��H1
S(g)��O2(g)===SO2(g) ��H2
��H1__________��H2
(2)CH4(g)��2O2(g)===CO2(g)��2H2O(l) ��H1
CH4(g)��2O2(g)===CO2(g)��2H2O(g) ��H2
��H1__________��H2
(3)4Al(s)��3O2(g)===2Al2O3(s) ��H1
4Fe(s)��3O2(g)===2Fe2O3(s) ��H2
��H1__________��H2
(4)ú��Ϊȼ����2��;����
;��1����ֱ��ȼ�գ�
C(s)��O2(g)===CO2(g) ��H1<0
;��2��������ˮú����
C(s)��H2O(g)===CO(g)��H2(g) ��H2>0
��ȼ��ˮú����
2CO(g)��O2(g)===2CO2(g) ��H3<0
2H2(g)��O2(g)===2H2O(g) ��H4<0
��H1����H2����H3����H4�Ĺ�ϵʽ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ����±���
Ԫ�ش��� | X | Y | Z | W |
ԭ�Ӱ뾶/pm | 160 | 143 | 70 | 66 |
��Ҫ���ϼ� | ��2 | ��3 | ��5����3����3 | ��2 |
����������ȷ����( )
A��X��YԪ�صĽ�����X<Y
B��һ�������£�Z������W�ij�������ֱ������ZW2
C��Y������������Ӧ��ˮ����������ϡ��ˮ
D��һ�������£�W���ʿ��Խ�Z���ʴ����⻯�����û�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���������У���ȷ����( )
A. 2��4-��������
B. 2��3��3-��������
C. 2-�һ�����
D. 2��3-��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com