
【题目】从宏观现象探究微观本质是重要的化学学科素养。以FeCl3溶液为实验研究对象,探究其与碱性物质之间的复杂多样性。实验如下:
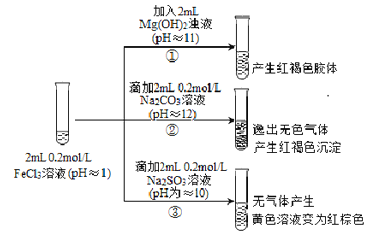
(1)①中反应的离子方程式是_________________。
(2)②中逸出的无色气体是_______________。
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
Ⅰ.甲取③中的红棕色溶液少许,滴入少量盐酸酸化的BaCl2溶液,产生白色沉淀。 甲得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是______________。
Ⅱ.乙认为甲的实验不严谨,重新设计并进行实验,证实了甲的结论是正确的。其实验方案是取Ⅰ中所得溶液少许进行__________离子的检验。
(4)受以上实验的启发,同学们对pH≈8的1mol/LNaF溶液与FeCl3溶液混合时的现象产生了好奇并进行实验:
实验操作及现象 | ④向2mL0.2mol/L FeCl3溶液中滴入2mL1mol/LNaF溶液。溶液变无色 |
⑤向2mL0.2mol/L FeCl3溶液中滴入2mL蒸馏水,溶液颜色变浅 |
Ⅰ.⑤的实验目的是___________。
Ⅱ.为探究④中溶液变无色的原因,进行如下实验:
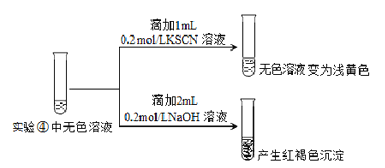
资料显示:FeF3溶液为无色。
用平衡移动原理解释红褐色沉淀产生的原因:_______________。
(5)根据实验,FeCl3溶液与碱性物质之间的反应的多样性与_____________________有关。
【答案】 3Mg(OH)2 +2Fe3+= 2Fe(OH)3(胶体)+ 3Mg2+ CO2 2Fe3+ + SO32- + H2O = 2Fe2+ + SO42- + 2H+ 亚铁离子(或Fe2+) 排除加水稀释对溶液颜色变化的影响 无色溶液中存在平衡:Fe3++ 3F-![]() FeF3,加入NaOH后,Fe3+更易与OH-结合生成难溶的Fe(OH)3 碱性物质的pH、离子的性质
FeF3,加入NaOH后,Fe3+更易与OH-结合生成难溶的Fe(OH)3 碱性物质的pH、离子的性质
【解析】(1)①中反应的离子方程式:3Mg(OH)2+2Fe3+=2Fe(OH)3(胶体)+3Mg2+;
(2)FeCl3溶液和Na2CO3溶液反应产生无色气体CO2和红褐色沉淀氢氧化铁;
(3)Ⅰ.三价铁离子能氧化SO32-,生成硫酸根离子,同时三价铁离子被还原为亚铁离子,其反应离子方程式为:2Fe3++SO32-+H2O=2Fe2++SO42-+2H+;
Ⅱ.乙认为甲的实验不严谨,重新设计并进行实验,证实了甲的结论是正确的.其实验方案是取Ⅰ中所得溶液少许进行亚铁离子(或Fe2+)的检验;
(4)Ⅰ.加水稀释对溶液颜色变化有影响;
Ⅱ.无色溶液中存在平衡:Fe3++3F-![]() FeF3,加入NaOH后,Fe3+更易与OH-结合生成难溶的Fe(OH)3;
FeF3,加入NaOH后,Fe3+更易与OH-结合生成难溶的Fe(OH)3;
(5)根据实验,FeCl3溶液与碱性物质之间的反应的多样性与碱性物质的pH、离子的性质有关。


科目:高中化学 来源: 题型:
【题目】为了探究化学反应速率和化学反应限度的有关问题,某研究小组进行了以下实验:
序号 | 反应温度/℃ | C(H2O2)/mol-L | V(H2O2)/mL | M(MnO2)/g | t/min |
1 | 20 | 2 | 10 | 0 | t1 |
2 | 20 | 2 | 10 | 0.1 | t2 |
3 | 20 | 4 | 10 | 0.1 | t3 |
4 | 40 | 2 | 10 | 0.1 | t4 |
(1)设计实验2和实验3的目的是研究_______对化学反应速率的影响。
(2)为研究温度对化学反应速率的影响,可以将实验_____和实验____作对比(填序号)。
(3)将实验1和实验2作对比,t1____t2(填“>”、“<”或“=”)。
II.以KI和FeCl3反应为例(2Fe3++2I-![]() 2Fe2++I2)设计实验,探究此反应存在一定的限度。可选试剂:①0.1mol·L-1KI溶液 ②0.1mol·L-1 FeCl3溶液③0.1mol·L-1 FeCl2溶液 ④0.1mol·L-1 HCl溶液⑤0.1mol·L-1 FeSCN溶液⑥ CCl4
2Fe2++I2)设计实验,探究此反应存在一定的限度。可选试剂:①0.1mol·L-1KI溶液 ②0.1mol·L-1 FeCl3溶液③0.1mol·L-1 FeCl2溶液 ④0.1mol·L-1 HCl溶液⑤0.1mol·L-1 FeSCN溶液⑥ CCl4
实验步骤:
(1)取5mL0.1mol·L-1KI溶液,再滴加几滴0.1mol·L-1 FeCl3溶液
(2)充分反应后,将溶液分成三份;
(3)取其中一份,加试剂⑥,振荡,CCl4层显紫色,说明反应生成碘;
(4)另取一份,加试剂_______(填序号),现象___________,说明此反应存在一定的限度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,影响一定质量气体体积大小的决定因素是( )
A.气体的密度 B.气体分子体积的大小
C.气体分子间的平均距离 D.气体的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯吡格雷是一种血小板聚集抑制剂,该药物以2-氯苯甲醛为原料的合成路线如下:
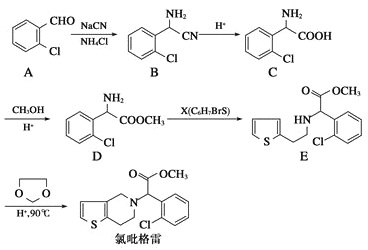
请根据以上信息,结合自己的掌握知识和具有的经验回答下列问题:
(1)分子C中除氯原子外的官能团名称为_________。
(2)X的结构简式为____________。
(3)D→E的反应类型是__________反应。
(4)分子C在一定条件下生成一种含有3个六元环的产物的化学方程式_________________
(5)同时满足下列两个条件的B的同分异构体共有____种(不包括B)
①与B含有相同的官能团 ②苯环上的取代基不超过2个。
(6)已知: ![]() 则由乙醇、甲醇为有机原料制备化合物
则由乙醇、甲醇为有机原料制备化合物![]() ,构成需要经历的反应类型有_______ (填写编号)。
,构成需要经历的反应类型有_______ (填写编号)。
①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应,写出制备化合物![]() 的最后一步反应________________
的最后一步反应________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是

A.液滴中的Cl― 由a区向b区迁移
B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-![]() 4OH-
4OH-
C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH―形成Fe(OH)2,进一步氧化、脱水形成铁锈
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e-![]() Cu2+
Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.10 mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随![]() 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( )

A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当lg![]() =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则 ![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol/L 的HA溶液中c(OH-)/c(H+)=1×10-8,下列叙述中正确的是( )
A.0.01 mol/L的HA溶液中c(H+)=1×10-4 mol/L
B.pH=3的HA溶液与pH=11的NaOH溶液等体积混合后所得溶液中:c(Na+)>c(A-)>c(OH-)>c(H+)
C.浓度均为0.1mol/L 的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则:c(OH-)-c(H+)<c(HA)-c(A-)
D.pH=3的HA溶液与pH=11的NaOH溶液按体积比1:10混合后所得溶液中:c(OH-)+c(A-)=c(H+)+c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从樟科植物枝叶提取的精油中含有甲、乙两种成分:
![]()
![]()
(1)①用酸性高锰酸钾溶液检验甲和乙中含有碳碳双键,方案是否可行 填“可行”或“不可行”)。
②请写出甲的一种能同时满足下列3个条件的同分异构体的结构简式 。
a.苯环上有两个不同的取代基
b.能与Br2的CCl4溶液发生加成反应
c.遇FeCl3溶液呈现紫色
(2)由甲转化为乙的过程为(已略去无关产物):

步骤Ⅰ的反应类型为 ,Y的结构简式 ,设计步骤Ⅰ的目的是 。
(3)1 mol乙最多可与 mol H2发生加成反应。
(4)写出乙与新制Cu(OH)2悬浊液反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com