
A、 四种基本反应类型与氧化还原反应的关系 |
B、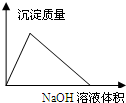 AlCl3溶液滴加NaOH溶液生成沉淀的情况 |
C、 Ba(OH)2溶液中滴加硫酸溶液导电性的情况 |
D、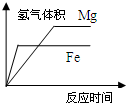 等体积等浓度稀硫酸分别与足量铁和镁反应的情况 |
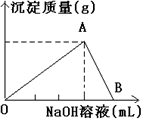 ,故B错误;
,故B错误;

科目:高中化学 来源: 题型:
| A、饱和石灰水中加入生石灰,若保持温度不变,则溶液中Ca2+的物质的量不变 |
| B、升高饱和石灰水的温度时,Ca(OH)2溶度积常数Ksp减小 |
| C、饱和石灰水中加入生石灰,若保持温度不变,则pH不变 |
| D、向饱和石灰水中加入浓CaCl2溶液会有Ca(OH)2沉淀析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 葡萄糖注射液 |
| 规格:250mL |
| 密度:1.08g?mL-1 |
| 生产批号:10032032 |
| 有效期:至2013年3月 |
| 质量分数:5% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1molCl2参加反应,转移的电子数一定为0.2NA |
| B、0.1molO2参加反应,转移的电子数一定为0.4NA |
| C、0.1molAl参加反应,转移的电子数一定为0.3NA |
| D、0.1molFe参加反应,转移的电子数一定为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| CuO |
| 高温 |
| H2O |
| Ca(OH)2 |
| 高温 |
| A、置换、化合、分解、复分解 |
| B、置换、化合、复分解、分解 |
| C、化合、置换、分解、复分解 |
| D、化合、置换、复分解、分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CuO+H2
| ||||
B、CaCO3
| ||||
| C、Na2O+H2O=2NaOH | ||||
| D、Al2O3+6HCl=2AlCl3+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、在pH=1的溶液中:NH
| ||||
B、有NO3-存在的强酸性溶液中:NH
| ||||
C、在c(H+)=1.0×10-13mol?L-1的溶液中:Na+、S2-、AlO
| ||||
D、有SO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com