
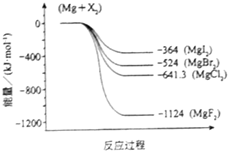
 金属镁是一种活泼的常见金属,有着广泛的用途.如图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态).
金属镁是一种活泼的常见金属,有着广泛的用途.如图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态).| ag |
| 24g/mol |
| a |
| 24 |
| a |
| 24 |
| 5a |
| 3 |
| a |
| 24 |
| 1 |
| 2 |
| a |
| 48 |
| a |
| 48 |
| 7a |
| 15 |
| 7a |
| 15 |
| 5a |
| 3 |
| 7a |
| 15 |
| b |
| 22.4 |
| 32b |
| 22.4 |
| 32b |
| 22.4 |
| b |
| 22.4 |
| 44b |
| 22.4 |
| 44b |
| 22.4 |
| 32b |
| 22.4 |
| 44b |
| 22.4 |
| 5a |
| 3 |
| ||
| 2 |
| 23a |
| 12 |
| 5a |
| 3 |
| 23a |
| 12 |
| 32b |
| 22.4 |
| 44b |
| 22.4 |
| 5a |
| 3 |
| 23a |
| 12 |


科目:高中化学 来源: 题型:阅读理解
 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.| A-B | A=B | A≡B | ||
| CO | 键能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| 键能差值(kJ?mol-1) | 441.2 273 | |||
| N2 | 键能(kJ?mol-1) | 154.8 | 418.3 | 941.7 |
| 键能差值(kJ?mol-1) | 263.6 523.3 | |||
查看答案和解析>>
科目:高中化学 来源:2011年福建省福州三中高考化学练习试卷(解析版) 题型:解答题
| A-B | A=B | A≡B | ||
| CO | 键能 | 357.7 | 798.9 | 1071.9 |
| 键能差值 | 441.2 273 | |||
| N2 | 键能 | 154.8 | 418.3 | 941.7 |
| 键能差值 | 263.6 523.3 | |||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com