
| A、是氧化剂 |
| B、是还原剂 |
| C、既是氧化剂又是还原剂 |
| D、既不是氧化剂又不是还原剂 |
科目:高中化学 来源: 题型:
| A、K2CO3、稀盐酸 |
| B、Na2CO3、稀盐酸 |
| C、Na2CO3、稀硫酸 |
| D、NaOH、稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
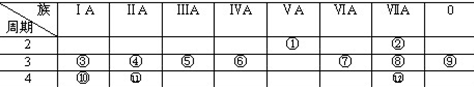
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验现象 | 原因分析 |
| A | 久置的浓硝酸呈黄色 | 浓硝酸不稳定,分解生成的NO2 溶解在其中 |
| B | 新制氯水中滴加石蕊试液,溶液先变红,后褪色 | 氯气与水反应生成HCl、HClO,呈酸性,使石蕊变红,HClO具有强氧化性、漂白性,使其褪色 |
| C | SO2通入溴水中,溴水褪色 | SO2具有漂白性,使其褪色 |
| D | 向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 | 在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、把pH=6的盐酸稀释1000倍 |
| B、把pH=8的NaOH溶液稀释10倍 |
| C、把10mL 1×10-5mol/L的H2SO4溶液与10mL 4×10-5mol/L的NaOH溶液相混合 |
| D、把c(OH-)=10-5mol/L的NaOH溶液10mL加到100mL浓度为10-4mol/L的NaOH溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2ω1=ω2 |
| B、2ω2=ω1 |
| C、ω2>2ω1 |
| D、2ω1>ω2>ω1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol Na作为还原剂失去的电子数为NA |
| B、在0℃,101 kPa时,22.4 L水中含有2NA个氢原子 |
| C、25℃,1.01×105Pa,64 g SO2中含有的原子数为NA |
| D、NA个一氧化碳分子和0.5 mol N2的质量比为2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com