
【题目】下列说法正确的是( )
A.汽油车在行驶过程中,热能首先转化为化学能,化学能再转化为动能
B.炸药发生爆炸时化学能完全转化为热能
C.炭燃烧时化学能主要转化为光能
D.柴草燃烧时,部分化学能转化为热能
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素。请回答:
(1)D在元素周期表中的位置是___________________________。
(2)C2B的电子式是__________________。
(3)B、C、E的离子半径由大到小的顺序为__________________(用化学式回答,下同);A、D、E元素最高价氧化物对应水化物的酸性由强到弱为_________________。
(4)B的气态氢化物与H2S相比沸点高的是_________(用化学式回答);原因是___________。
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来除去水中超标的Mn2+,生成黑色沉淀MnO2,当消耗13.50gEB2时,共转移了1mol电子,则反应的离子方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯度晶体硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场 “革命”。它的制备方法如下图所示,下列说法正确的是
![]()
A. 步骤①的化学方程式为:SiO2+C![]() Si+CO2↑
Si+CO2↑
B. 灼烧熔融的Na2CO3固体,可用石英坩埚
C. 二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D. SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点67.6℃),可通过蒸馏(或分馏)提纯SiHCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的两种氧化物在化工生产中都有着重要的用途。
I.CuO可用于制备Cu2O。
已知:①2Cu2O(s)![]() 4Cu(s)+O2(g) △H1=+338kJ·mol-1;
4Cu(s)+O2(g) △H1=+338kJ·mol-1;
②2CuO(s)![]() 2Cu(s)+O2(g) △H2=+314kJ·mol-1。
2Cu(s)+O2(g) △H2=+314kJ·mol-1。
(1)CuO分解生成2molCu2O的热化学方程式为____________________________________。
(2)温度为T时,向5L恒容密闭容器中加人80g CuO制备Cu2O,5min时恰好达到平衡,测得容器中Cu2O的物质的量为0.4mol。
①该反应的平衡常数K=_____________________。
②5min时缩小容器容积,重新达到平衡时O2的浓度_________(填“增大”“减小”或“不变”)。
③其他条件不变,起始向该容器中充入0.5molCuO,重复实验,达到平衡的时间_____2.5min(填“大于”“小于”或“等于”);达到平衡时Cu2O的物质的量______0.2mol(填“大于”“小于”或“等于”)。
(3)研究表明,在CuO中加入适量碳粉,下列说法中有利于制得纳米级Cu2O的是_____(填选项字母)。
A.碳与氧气反应放热,加快反应速率
B.生成CO气体,使固体颗粒容易分散
C.CO可以将Cu2O还原为铜粉
D.CO作该反应的催化剂
II.CuO可用于冶炼铜(已知:CO的燃烧热△H=-283kJ/mol),一定条件下,将1molCuO和0.5molCO加人2L密闭容器中发生反应,t1时达到平衡,t2后改变容器中的条件,用CO表示的反应速率(v)与时间(t)的关系如图所示(三个阶段改变的条件为温度、压强、浓度中的一个)。
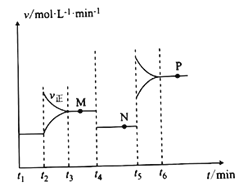
(4)t4时改变的条件为______________________________________________。
(5)M、N、P三点对应状态下,CO的转化率a(M)、a(N)、a(P)的大小关系为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeC13、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
A.溶液中一定不含Cu2+B.溶液中一定含Fe2+
C.加入KSCN溶液一定不变红色D.剩余固体中可能含有Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向饱和氯水中逐滴滴入0.1mol·L-1的氢氧化钠溶液,pH变化如右图所示,下列有关叙述正确的是( )
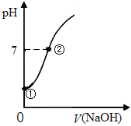
A. ①点所示溶液中只存在HClO的电离平衡
B. ①到②水的电离程度逐渐减小
C. I-能在②点所示溶液中存在
D. ②点所示溶液中:c(Na+)=c(Cl-) + c(ClO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定条件下N2与H2反应生成NH3,请回答:
①若反应物的总能量为E1,生成物的总能量为E2,且E1>E2,则该反应为________(填“吸热”或“放热”)反应。
②已知拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___________________________________________。
(2)实验室用50mL0.50mol·L-1盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有两处明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称为___________________________;实验室提供了0.50mol·L-1和0.55mol·L-1两种浓度的NaOH溶液,应选择___________mol·L-1的NaOH溶液进行实验。

(3)人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如下:

①在阳极区发生的反应包括__________________________________和H++HCO===H2O+CO2↑。
②简述CO![]() 在阴极区再生的原理:____________________________________。
在阴极区再生的原理:____________________________________。
(4)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,试计算溶液中![]() =_______。(常温下H2SO3的电离平衡常数Ka1=1.0×10-2,Ka2=6.0×10-8)
=_______。(常温下H2SO3的电离平衡常数Ka1=1.0×10-2,Ka2=6.0×10-8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系不正确的是
A. ![]() B.
B. ![]() C. n=m+17Vc D.
C. n=m+17Vc D. ![]() m<p<
m<p<![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置可间接氧化工业废水中含氮离子(NH4+)。下列说法不正确的是
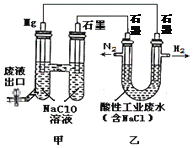
A. 乙是电能转变为化学能的装置
B. 含氮离子氧化时的离子方程式为:3Cl2 + 2NH4+=N2 + 6Cl-+8H+
C. 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH减小
D. 电池工作时,甲池中的Na+移向Mg电极
【答案】D
【解析】A、甲中活泼金属镁作原电池的负极,石墨为正极形成原电池,乙是连接原电池的电解池,电解酸性工业废水,电解池是将电能转变为化学能的装置,选项A正确;B、酸性条件下含氮离子氧化时转化为氮气,反应的离子方程式为:3Cl2 + 2NH4+=N2 + 6Cl-+8H+,选项B正确;C、若生成H2和N2的物质的量之比为3:1,根据电极反应6H++6e-=3H2↑、3Cl2 + 2NH4+=N2 + 6Cl-+8H+,则处理后废水的H+浓度增大,pH减小,选项C正确;D、电池工作时,甲池是原电池,原电池中阳离子Na+移向正极石墨电极,选项D不正确。答案选D。
【题型】单选题
【结束】
7
【题目】已知某透明澄清的溶液中可能含有NO3- 、Cl- 、SO42-、CO32-、NH4+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液的成分,某学习小组做了如下实验:①取该溶液100mL,加入过量NaOH溶液,加热得到0.02mol气体,同时产生红褐色沉淀; ②将沉淀过滤、洗涤、灼烧,得到1.6 g固体; ③向上述滤液中加入足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。下列说法正确的是
A. 不能确定原溶液中是否含有Al3+和K+
B. 原溶液中含有的离子只有:Cl- 、SO42-、NH4+、Fe3+
C. 原溶液中c(NO3-)=0.2 mol·L-1 c(Fe3+)=0.2 mol·L-1
D. 在原溶液中加入足量的铁粉所得溶液中阳离子所带正电荷数减少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com