
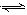 2AB2(g),△H<0,下列说法正确的是()。
2AB2(g),△H<0,下列说法正确的是()。科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
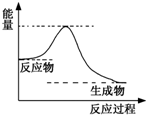
已知反应:A2(g)+2B2(g)![]() 2AB2(g),△H>0,下列说法正确的是 ( )
2AB2(g),△H>0,下列说法正确的是 ( )
A.升高温度正反应速率加快,逆反应速率减慢
B.0.1molA2和0.2molB2反应达到平衡时生成0.2molAB2
C.达平衡后,升高温度,正、逆反应速率均加快,B的转化率不变
D.催化剂可同等程度改变正逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
A、D、E、M、L是原子序数依次增大的五种短周期元素。已知A是元素周期表中原子半径最小的元素;D的某种单质是天然存在的最硬物质;E是地壳中含量最多的元素;M与A位于同一主族;L与M能够形成ML型离子化合物。回答下列问题:
(1)元素D在元素周期表中的位置是 。
(2)L的单质与M的最高价氧化物对应水化物反应的离子方程式为 。
(3)由A、D组成的最简单化合物甲的二氯化物有 种。人们已经研究出以甲为燃料的新型碱性燃料电池,写出该电池正极的电极反应式为: 。
(4)已知反应:DE(g)+A2E(g)![]() DE2(g)+A2(g),
DE2(g)+A2(g),
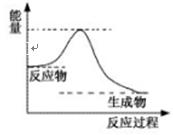
一定条件下该反应进行过程中的能量变化如上图表示,请结合上图判断:该反应△H 0(填“>”、“<”或“=”)。该反应的平衡常数表达式为:K= 。
(5)25℃时,物质的量浓度相同的MEA、MADE3、MLE三种溶液,水的电离程度由大到小的顺序为 。
查看答案和解析>>
科目:高中化学 来源:2011届福建省莆田市高三教学质量检查化学试卷 题型:填空题
(11分)A、D、E、M、L是原子序数依次增大的五种短周期元素。已知A是元素周期表中原子半径最小的元素;D的某种单质是天然存在的最硬物质;E是地壳中含量最多的元素;M与A位于同一主族;L与M能够形成ML型离子化合物。回答下列问题:
(1)元素D在元素周期表中的位置是 。
(2)L的单质与M的最高价氧化物对应水化物反应的离子方程式为 。
(3)由A、D组成的最简单化合物甲的二氯化物有 种。人们已经研究出以甲为燃料的新型碱性燃料电池,写出该电池正极的电极反应式为: 。
(4)已知反应:DE(g)+A2E(g) DE2(
DE2( g)+A2(g),
g)+A2(g),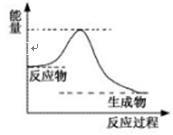
一定条件下该反应进行过程中的能量变 化如上图表示,请结合上图判断:该反应△H 0(填“>”、“<”或“=”)。该反应的平衡常数表达式为:K=
化如上图表示,请结合上图判断:该反应△H 0(填“>”、“<”或“=”)。该反应的平衡常数表达式为:K=  。
。
(5)25℃时,物质的量浓度相同的MEA、MADE3、MLE三种溶液,水的电离程度由大到小的顺序为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com