
(17分)下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备和A中加热装置已省略)。
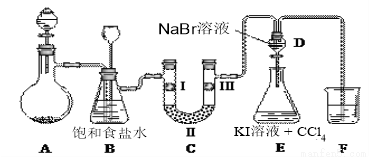
(1)制备氯气选用的药品为:二氧化锰和浓盐酸,相关反应的化学方程式为: 。
(2)装置B中饱和食盐水的作用是 ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象 。
(3)装置F烧杯中盛放的试剂是 ,其中发生反应的离子方程式是 。
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入 。
选项 | I | II | III |
A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
B | 干燥的有色布条 | 硅胶 | 湿润的有色布条 |
C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
D | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)设计装置D、E的目的是比较Cl2、Br2、I2的氧化性强弱。当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为红棕色,说明Cl2的氧化性大于Br2。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是 。该现象 (填“能”或“不能”)说明Br2的氧化性强于I2,原因是 。
(1) MnO2+4HCl(浓) 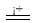 MnCl2+Cl2↑+2H2O (2)除去Cl2中的HCl B中长颈漏斗中液面上升,形成水柱 (3)NaOH溶液 2OH-+Cl2=Cl-+ClO-+H2O (4)D (5)E中溶液分为两层,下层(CCl4层)为紫红色 不能 过量的Cl2也可将I-氧化为I2
MnCl2+Cl2↑+2H2O (2)除去Cl2中的HCl B中长颈漏斗中液面上升,形成水柱 (3)NaOH溶液 2OH-+Cl2=Cl-+ClO-+H2O (4)D (5)E中溶液分为两层,下层(CCl4层)为紫红色 不能 过量的Cl2也可将I-氧化为I2
【解析】
试题分析:(1)二氧化锰和浓盐酸反应的方程式为MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O;(2)从A中出来的气体含有氯化氢,所以饱和食盐水的作用是除去Cl2中的HCl;发生堵塞时B中压强增大,B中长颈漏斗中液面上升,形成水柱;(3)氯气有毒,为防止空气污染,用氢氧化钠溶液吸收,所以F中盛放的试剂是NaOH溶液;发生反应的离子方程式是2OH-+Cl2=Cl-+ClO-+H2O;(4) 为验证氯气是否具有漂白性,C中I、II、III依次放入:湿润的有色布条、无水氯化钙、干燥的有色布条;(5)将装置D中少量溶液加入装置E中,I—被氧化为I2,所以E中溶液分为两层,下层(CCl4层)为紫红色;过量的Cl2也可将I-氧化为I2,该现象不能说明Br2的氧化性强于I2。
MnCl2+Cl2↑+2H2O;(2)从A中出来的气体含有氯化氢,所以饱和食盐水的作用是除去Cl2中的HCl;发生堵塞时B中压强增大,B中长颈漏斗中液面上升,形成水柱;(3)氯气有毒,为防止空气污染,用氢氧化钠溶液吸收,所以F中盛放的试剂是NaOH溶液;发生反应的离子方程式是2OH-+Cl2=Cl-+ClO-+H2O;(4) 为验证氯气是否具有漂白性,C中I、II、III依次放入:湿润的有色布条、无水氯化钙、干燥的有色布条;(5)将装置D中少量溶液加入装置E中,I—被氧化为I2,所以E中溶液分为两层,下层(CCl4层)为紫红色;过量的Cl2也可将I-氧化为I2,该现象不能说明Br2的氧化性强于I2。
考点:本题考查综合实验。


科目:高中化学 来源:2014-2015学年福建省厦门市高三质量检查理综化学试卷(解析版) 题型:选择题
在密闭容器中,5 mol H2与2 mol CO2发生反应:3H2(g)十CO2(g)≒CH3OH(g)+H2O(g)反应达到平衡时,改变温度(T)和压强(P),反应混合物中甲醇(CH3OH)的物质的量分数变化情况如图所示下列说法错误的是

A.P1> P2> P3>P4
B.甲醇的物质的量分数越高,反应的平衡常数越大
C.若T1> T2> T3>T4,则该反应为放热反应
D.T4、P4、时,H2的平衡转化率为60%
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省深圳市南山区上学期高一化学期末试卷(解析版) 题型:选择题
根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是
①I2 + SO2 + 2H2O = H2SO4 + 2HI
②2FeCl2 + Cl2 = 2FeCl3
③2FeCl3 + 2HI = 2FeCl2 + 2HCl+I2
A.SO2>I->Fe2+>Cl- B.Cl->Fe2+>SO2>I-
C.Fe2+>I->Cl->SO2 D.I->Fe2+>Cl->SO2
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市等三校高二上学期期末化学试卷(解析版) 题型:选择题
下列水解的离子方程式正确的是
A.S2﹣+2H2O H2S+2OH﹣ B.Fe3++3H2O
H2S+2OH﹣ B.Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
C.HCO3﹣+H2O CO32﹣+H3O+ D.HS﹣+H2O
CO32﹣+H3O+ D.HS﹣+H2O H2S ↑ + OH﹣
H2S ↑ + OH﹣
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市等三校高二上学期期末化学试卷(解析版) 题型:选择题
下列有关金属腐蚀与防护的说法正确的是
A.银器表面在空气中因电化腐蚀渐渐变暗
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省揭阳市高一上学期期末考试化学试卷(解析版) 题型:选择题
研究表明:多种海产品体内含有+5价的砷(As)元素,对人体无毒,而砒霜的成分是As2O3,有剧毒;青菜中含有维生素C。专家忠告:不要同时大量食用海鲜和青菜,否则容易中毒。下面有关解释正确的是
A.As2O3中As元素为+3价 B.维生素C能将+5价砷还原成As2O3
C.致人中毒过程中砷发生氧化反应 D.维生素C具有氧化性
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省揭阳市高二上学期期末考试化学文试卷(解析版) 题型:?????
对于合金的说法,正确的是
A.常见的铜合金是青铜和黄铜
B.合金与各组分金属相比一般具有更低的熔点
C.钢是铁和碳的合金,生铁则是纯铁
D.合金与各组分金属相比一般具有更大的硬度
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省揭阳市高二上学期期末考试化学文试卷(解析版) 题型:?????
常温下,2L物质的量浓度为0.5mol·L-1K2SO4溶液含有
A.0.5mol的SO42- B.0.5mol的K+
C.1.0mol的K+ D.96g的SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com