
【题目】X、Y、Z、W为原子序数依次增大的四种短周期元素,其中X元素原子的核外电子总数等于其电子层数, X与Y、W可分别形成YX3和XW型共价化合物,YX3极易溶于水, Z元素是地壳中含量最高的金属元素,W 的原子半径是第三周期中最小的。
(1)写出YX4+的电子式_______。
(2)写出Z与W所形成的盐与 YX3的水溶液反应的离子方程式________________。
(3)室温下,pH=3的XW溶液与pH=5的YX4W溶液中由水电离出的c(H+)的比为___。
(4)已知X单质和Y单质反应生成YX3的反应是可逆反应,ΔH<0, 将X、Y的两种单质以等物质的量充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。下列说法正确的是_____________________。
a.达到化学平衡时,任何一种物质表示的正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,X、Y两种单质在混合气体中的物质的量之比为1∶1
d.达到化学平衡的过程中混合气体的平均相对分子质量减小
(5)有人设想寻求合适的催化剂和电极材料,以Y2、X2为电极反应物,以XW-YX4W 为电解质溶液制备新型燃料电池。请写出该电池的正极反应式_____________。
(6)汽车尾气中含有CO、NO、NO2等有毒气体,对汽车加装尾气净化装置,用含铂等过渡元素的催化剂催化,可使有毒气体相互反应转化成无毒气体。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+68 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-221 kJ·mol-1
C(s)+O2(g)=CO2 (g) ΔH3=-393.5 kJ·mol-1
CO与NO2反应的热化学方程式为____________________,反应一定条件下可逆,温度不同(T2>T1二者均大于常温)、其他条件相同,下列图像正确的是______。

【答案】 略 Al3+ +3NH3·H2O =Al(OH)3↓+3NH4 + 1:106 ab N2+6e-+8H+=2NH4+ 4CO(g)+ 2NO2(g)=4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1 乙
【解析】本题考查元素周期表和元素周期律的应用,以及化学反应原理的应用,X元素原子的核外电子总数等于其电子层数,即X为H,X与Y、W可分别形成YX3和XW型共价化合物,YX3极易溶于水,推出YX3为NH3,即Y为N,W位于VIIA,Z元素是地壳中含量最高的金属元素,即Z为Al,W为Cl,(1)YX4+为NH4+,其电子式为:![]() ;(2)Z与W形成的盐为AlCl3,YX3为NH3,因此反应的离子方程式为: Al3++3NH3·H2O=Al(OH)3↓+3NH4+;(3)pH=3的盐酸溶液中:水电离出的c(H+)等于水电离出的c(OH-),水电离出的c(H+)=c(OH-)=Kw/c(H+)=10-14/10-3mol·L-1=10-11mol·L-1,pH=5的NH4Cl溶液中,H+完全是由水电离产生,因此水电离出c(H+)=10-5mol·L-1,因此两者的比值为10-11:10-5=1:106;(4)发生的反应是N2+3H2
;(2)Z与W形成的盐为AlCl3,YX3为NH3,因此反应的离子方程式为: Al3++3NH3·H2O=Al(OH)3↓+3NH4+;(3)pH=3的盐酸溶液中:水电离出的c(H+)等于水电离出的c(OH-),水电离出的c(H+)=c(OH-)=Kw/c(H+)=10-14/10-3mol·L-1=10-11mol·L-1,pH=5的NH4Cl溶液中,H+完全是由水电离产生,因此水电离出c(H+)=10-5mol·L-1,因此两者的比值为10-11:10-5=1:106;(4)发生的反应是N2+3H2 ![]() 2NH3,a、根据化学平衡状态的定义,一定条件下,当正反应速率等于逆反应速率,说明反应达到平衡状态,故a正确;
2NH3,a、根据化学平衡状态的定义,一定条件下,当正反应速率等于逆反应速率,说明反应达到平衡状态,故a正确;
b、N2+3H2 ![]() 2NH3
2NH3
起始: 1 1 0
变化: x 3x 2x
任意时刻:1-x 1-3x 2x
N2的体积分数等于其物质的量分数,即为![]() ,故b正确;c、根据b选项分析,达到平衡时,两者气体物质的量比值为(1-3x):(1-x),故c错误;d、根据M=m/n,组分都是气体,因此气体质量不变,反应向正反应方向进行,气体物质的量减小,即M增大,故d错误;(5)以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液,根据原电池的工作原理,电池正极上得到电子,化合价降低,发生还原反应,因此N2在正极上反应,即电极反应式为:N2+6e-+8H+=2NH4+;(6)根据盖斯定律,①N2(g)+2O2(g)=2NO2(g) ,②2C(s)+O2(g)=2CO(g) ,③C(s)+O2(g)=CO2 (g),CO和NO2发生的反应是4CO+2NO2=N2+4CO2,③×4-②×2-①得出△H=(-393.5×4+221×2-68)kJ·mol-1=-1200kJ·mol-1,热化学反应方程式为: 4CO(g)+ 2NO2(g)=4CO2(g)+N2(g) ΔH=-1200kJ·mol-1;甲图像:因为T2>T1,升高温度,正逆反应速率都增大,故甲图错误;乙图像:温度升高,化学反应速率加快,首先达到平衡,此反应属于放热反应,升高温度,平衡向逆反应方向移动,NO2的转化率降低,故乙图像正确;丙图像:加压,平衡向体积减小方向移动,即增大压强,平衡向正反应方向移动,CO体积分数随着压强的增大而减小,故丙图像错误。
,故b正确;c、根据b选项分析,达到平衡时,两者气体物质的量比值为(1-3x):(1-x),故c错误;d、根据M=m/n,组分都是气体,因此气体质量不变,反应向正反应方向进行,气体物质的量减小,即M增大,故d错误;(5)以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液,根据原电池的工作原理,电池正极上得到电子,化合价降低,发生还原反应,因此N2在正极上反应,即电极反应式为:N2+6e-+8H+=2NH4+;(6)根据盖斯定律,①N2(g)+2O2(g)=2NO2(g) ,②2C(s)+O2(g)=2CO(g) ,③C(s)+O2(g)=CO2 (g),CO和NO2发生的反应是4CO+2NO2=N2+4CO2,③×4-②×2-①得出△H=(-393.5×4+221×2-68)kJ·mol-1=-1200kJ·mol-1,热化学反应方程式为: 4CO(g)+ 2NO2(g)=4CO2(g)+N2(g) ΔH=-1200kJ·mol-1;甲图像:因为T2>T1,升高温度,正逆反应速率都增大,故甲图错误;乙图像:温度升高,化学反应速率加快,首先达到平衡,此反应属于放热反应,升高温度,平衡向逆反应方向移动,NO2的转化率降低,故乙图像正确;丙图像:加压,平衡向体积减小方向移动,即增大压强,平衡向正反应方向移动,CO体积分数随着压强的增大而减小,故丙图像错误。


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质分子结构特征的描述,正确的是
A. 乙炔易与溴的四氯化碳溶液发生反应,且lmol乙炔完全加成消耗2molBr2,证明乙炔分子里含有一个碳碳三键
B. 苯分子的结构中存在碳碳单键和碳碳双键交替出现的结构
C. 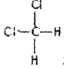 和
和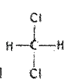 属于同一种物质,不能用来解释甲烷是一种正四面体结构
属于同一种物质,不能用来解释甲烷是一种正四面体结构
D. lmolCH3CH2OH与Na完全反应只生成0.5molH2,不能说明乙醇分子中有一个氢原子与其它氢原子不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某液体化合物X2Y4 , 常用做火箭燃料.16g X2Y4在一定量的O2中恰好完全燃烧,反应方程式为X2Y4(l)+O2(g)═X2(g)+2Y2O(l).冷却后标准状况下测得气体生成物的体积为11.2L,其密度为1.25gL﹣1 , 则:
(1)反应前O2的体积V(O2)为;
(2)X2的摩尔质量为;Y元素的名称是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.葡萄糖与果糖、淀粉与纤维素均互为同分异构体
B.纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应
C.糖、油脂、蛋白质均不溶于水
D.淀粉、纤维素、蛋白质都是天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中,a、b、c、d、e为元素周期表中前四周期的一部分元素,下列有关叙述正确的是( ) 
A.元素c和d的最高价氧化物对应水化物的酸性:c>d
B.五种元素中,元素e的性质最稳定
C.元素b位于ⅥA族,有+6、﹣2两种常见化合价
D.元素c和e的气态氢化物的稳定性:c>e
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PETG是一种新型材料,可回收利用,对环境不构成任何威胁,其结构简式如下: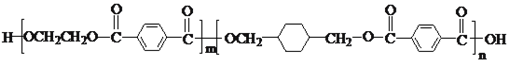 ,已知:RCOOR1+R2OH―→RCOOR2+R1OH(R、R1、R2表示烃基)。采用如下图所示的合成路线可合成PETG:
,已知:RCOOR1+R2OH―→RCOOR2+R1OH(R、R1、R2表示烃基)。采用如下图所示的合成路线可合成PETG:

试回答下列问题:
(1)试剂X为______________;反应⑦的反应类型为_______________。
(2)写出物质H的名称________________________。
(3)写出结构简式: I_____________________________。
(4)写出反应⑤的化学方程式:_________________________________________。
(5)合成时应控制的单体的物质的量n (D)∶n (F)∶n (H)=__________(用m、n表示)。
(6)同时符合下列要求的物质H的同分异构体共有__________种。
①遇FeCl3溶液显紫色;②能与NaHCO3溶液反应,并有气体放出;③能发生银镜反应。
(7)已知:![]() 请写出由D及其它必要物质可合成
请写出由D及其它必要物质可合成![]() 的反应历程。________________
的反应历程。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同体积0.3 mol·L-1的H2SO4、HCl、HNO3、CH3COOH溶液中,加入足量的Zn,下列说法中正确的是( )
A. 硫酸中放出氢气最快 B. 醋酸中放出氢气量最多
C. 盐酸与醋酸放出氢气的初始速率相同 D. 盐酸和硝酸中放出的氢气相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com