
| A. | 滴定前,滴定管尖嘴部分有气泡,滴定后气泡消失 | |
| B. | 锥形瓶沾有少量水 | |
| C. | 以甲基橙作指示剂 | |
| D. | 滴定前仰视滴定管读数,滴定后平视刻度读数 |
分析 根据酚酞在碱性变色范围内变色以及根据c(待测)=$\frac{c(标准)V(标准)}{V(待测)}$来分析.
解答 解:A、滴定前,滴定管尖嘴部分有气泡,滴定后气泡消失,NaOH溶液体积偏多,根据c(待测)=$\frac{c(标准)V(标准)}{V(待测)}$,c(待测)偏高,故A错误;
B、锥形瓶沾有少量水,待测液的物质的量不变,NaOH溶液体积不变,根据c(待测)=$\frac{c(标准)V(标准)}{V(待测)}$,c(待测)不变,故B错误;
C、甲基橙在酸性变色范围变色,变色范围是3.1-4.4,滴定终点时溶液呈酸性,NaOH溶液体积偏少,根据c(待测)=$\frac{c(标准)V(标准)}{V(待测)}$,c(待测)偏低,故C正确;
D、滴定前仰视滴定管读数,滴定后平视刻度读数,NaOH溶液体积偏小,根据c(待测)=$\frac{c(标准)V(标准)}{V(待测)}$,c(待测)偏小,故D正确;
故选CD.
点评 本题考查中和滴定的误差分析,注意利用公式来分析解答,无论哪一种类型的误差,都可以归结为对标准溶液体积的影响,其标准溶液的体积偏小,那么测得的物质的量的浓度也偏小;其标准溶液的体积偏大,那么测得的物质的量的浓度也偏大,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 溶液pH:NaF>NaCN | B. | n1>n2 | ||
| C. | H2O的电离程度:NaF>NaCN | D. | c(F-)<c(CN-) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 过滤 萃取 分液 | B. | 萃取 分液 蒸馏 | C. | 分液 蒸馏 萃取 | D. | 萃取 蒸馏 分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
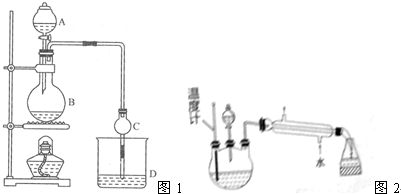
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 测定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 第一次 | 25.00 | 0.40 | 20.38 |
| 第二次 | 25.00 | 4.00 | 24.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
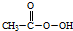 (过氧乙酸)+H2O
(过氧乙酸)+H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现使用酸碱中和滴定法测定市售白醋的总酸量(g•100mL-1).
现使用酸碱中和滴定法测定市售白醋的总酸量(g•100mL-1).| 滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
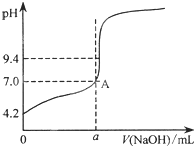 现用邻苯二甲酸氢钾标准溶液来测定NaOH溶液的浓度.用氢氧化钠溶液来滴定邻苯二甲酸溶液时有下列操作:
现用邻苯二甲酸氢钾标准溶液来测定NaOH溶液的浓度.用氢氧化钠溶液来滴定邻苯二甲酸溶液时有下列操作:| 滴定次数 实验数据 | 1 | 2 | 3 | 4 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.10 | 0.30 | 0.00 | 0.20 |
| V(NaOH)/mL(终读数) | 20.08 | 20.30 | 20.80 | 20.22 |
| V(NaOH)/mL(消耗) | 19.98 | 20.00 | 20.80 | 20.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
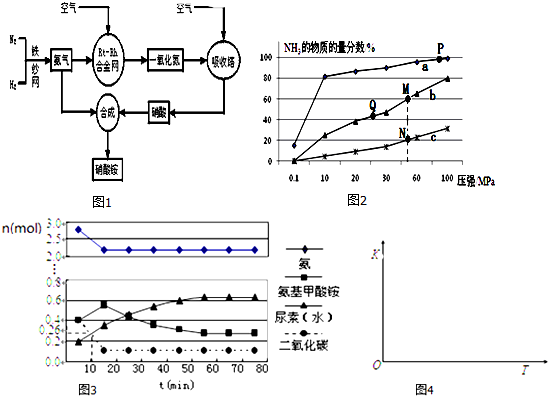
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com