���𰸡�
������XԪ����Ҫ���ϼ�-2��ԭ�Ӱ뾶Ϊ0.0074nm��XΪ��Ԫ�أ�YԪ����������������������������֮��Ϊ4��Y���ڵ������ڵڢ�A���ڶ����ڵڢ�A�壬ΪCl��O��XΪ��Ԫ�أ���YΪClԪ�أ�ZԪ�ص�����������ȼ�գ����������������������֮һ����ZΪ��Ԫ�أ�DԪ������������Ӧ��ˮ�����ܵ������������ȵ����������ӣ�DΪNaԪ�أ�EԪ�ص����������еij�������������Ʒ�ڳ�ʪ�������ױ���ʴ������EΪFeԪ�أ�
��1��ʵ�����ڶ������������������·ֽ�H
2O
2�Ʊ�O
2��
��2��ͬ����������ҷǽ�������ǿ���ǽ�����Խǿ�⻯��Խ�ȶ���
��3��EԪ����YԪ�ؿ��γ�FeCl
2��FeCl
3��
�������ӡ�������������Һ�ж�ˮ�⣬����Ӧ�����ᣬ������ˮ�⣻
������������Ӧ����FeCl
3������ֱ������FeCl
2��
��ͭƬ��̼����FeCl
3��Һ���ԭ��أ�ͭΪ������ʯīΪ�����������ɸ��������ص�������������
�ܵ��Ӳ�ṹ��ͬ�˵����Խ�����Ӱ뾶ԽС��������������ͬ���Ӳ�Խ�����Ӱ뾶Խ��
��4��Y�����������ΪCl
2O
7��Ϊ��ɫҺ�壬��0.25mol��������һ������ˮ��ϵõ�һ��ϡ��Һ���ų�QkJ����������ΪHClO
4��Һ��1molCl
2O
7��l����Ӧ�ų�����Ϊ4QkJ������Ȼ�ѧ����ʽ��дԭ����д��
��5��Fe�ڳ�ʪ�Ŀ����з�����ʴʱ����Ҫ����������ʴ�������������ŵ�������������
��6���ȼҵ����ȡ����Cl
2���ʣ�������ӦΪ2NaCl+2H
2O

H
2��+Cl
2��+2NaOH�������������������������ʵ������ٸ���V=nVm�������������
����⣺XԪ����Ҫ���ϼ�-2��ԭ�Ӱ뾶Ϊ0.0074nm��XΪ��Ԫ�أ�YԪ����������������������������֮��Ϊ4��Y���ڵ������ڵڢ�A���ڶ����ڵڢ�A�壬ΪCl��O��XΪ��Ԫ�أ���YΪClԪ�أ�ZԪ�ص�����������ȼ�գ����������������������֮һ����ZΪ��Ԫ�أ�DԪ������������Ӧ��ˮ�����ܵ������������ȵ����������ӣ�DΪNaԪ�أ�EԪ�ص����������еij�������������Ʒ�ڳ�ʪ�������ױ���ʴ������EΪFeԪ�أ�
��1��ʵ���ҿ�������H
2O
2�ֽ��Ʊ�O
2����Ӧ����ʽΪ��2H
2O
2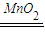
2H
2O+O
2�����ʴ�Ϊ��2H
2O
2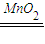
2H
2O+O
2����
��2���ǽ�����Cl��S���ǽ�����Խǿ�⻯��Խ�ȶ������ȶ��ԣ�HCl��H
2S���ʴ�Ϊ��HCl��H
2S��
��3��EԪ����YԪ�ؿ��γ�FeCl
2��FeCl
3��
�������ӡ�������������Һ�ж�ˮ�⣬����FeCl
2��FeCl
3��Һ��һ�㽫FeCl
2��FeCl
3�ܽ���������Һ�У��ʢ٢�����������Ӧ����FeCl
3������ֱ������FeCl
2���ʢ���ȷ��
��ͭƬ��̼����FeCl
3��Һ���ԭ��أ�ͭΪ������������ͭƬ�ص�������̼�����ʢ���ȷ��
�ܵ��Ӳ�ṹ��ͬ�˵����Խ�����Ӱ뾶ԽС��������������ͬ���Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶S
2-��Cl
-��Na
+����Z��Y��D�����Ӱ뾶��С���μ�С���ʢܴ���
�ʴ�Ϊ���ڢۣ�
��4��Y�����������ΪCl
2O
7��Ϊ��ɫҺ�壬��0.25mol��������һ������ˮ��ϵõ�HClO
4ϡ��Һ���ų�QkJ���������ʸ÷�Ӧ���Ȼ�ѧ����ʽΪCl
2O
7��l��+H2O��l��=HClO
4��aq����H=-4QkJ/mol��
�ʴ�Ϊ��Cl
2O
7��l��+H2O��l��=HClO
4��aq����H=-4QkJ/mol��
��5��Fe�ڳ�ʪ�Ŀ����з�����ʴʱ����Ҫ����������ʴ�������������ŵ������������������缫��ӦʽΪO
2+2H
2O+4e
-=4OH
-��
�ʴ�Ϊ��O
2+2H
2O+4e
-=4OH
-��
��6���ȼҵ����ȡ����Cl
2���ʣ�������ӦΪ2NaCl+2H
2O

H
2��+Cl
2��+2NaOH������·��ͨ��amol����ʱ����������Ϊ0.5amol����������Ϊ0.5amol������������������amol�����Ϊamol×22.4L/mol=22.4aL���ʴ�Ϊ��22.4a��
���������⿼��Ԫ���ƶϡ�Ԫ�������ɡ�Fe��Ԫ�ػ��������ʡ��Ȼ�ѧ����ʽ��д��ԭ��ء����صȣ���Ŀ��Ϊ�ۺϣ��Ƕ�ѧ���ۺ������Ŀ��飬�ѶȲ���

 H2��+Cl2��+2NaOH�������������������������ʵ������ٸ���V=nVm�������������
H2��+Cl2��+2NaOH�������������������������ʵ������ٸ���V=nVm�������������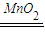 2H2O+O2�����ʴ�Ϊ��2H2O2
2H2O+O2�����ʴ�Ϊ��2H2O2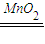 2H2O+O2����
2H2O+O2���� H2��+Cl2��+2NaOH������·��ͨ��amol����ʱ����������Ϊ0.5amol����������Ϊ0.5amol������������������amol�����Ϊamol×22.4L/mol=22.4aL���ʴ�Ϊ��22.4a��
H2��+Cl2��+2NaOH������·��ͨ��amol����ʱ����������Ϊ0.5amol����������Ϊ0.5amol������������������amol�����Ϊamol×22.4L/mol=22.4aL���ʴ�Ϊ��22.4a��

 ����ʦ���һ��һ��ϵ�д�
����ʦ���һ��һ��ϵ�д� �Ͻ�ƽ��У����ϵ�д�
�Ͻ�ƽ��У����ϵ�д�



 �й�Ԫ��X��Y��Z��D��E����Ϣ����
�й�Ԫ��X��Y��Z��D��E����Ϣ����
