
在25℃、101kPa条件下,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5kJ/mol、285.8kJ/mol、870.3kJ/mol,则2C(s)+2H2(g)+O2(g)═CH3COOH(l)的反应热为( )
|
| A. | ﹣488.3 kJ/mol | B. | +488.3 kJ/mol |
|
| C. | ﹣191 kJ/mol | D. | +191 kJ/mol |
考点:
用盖斯定律进行有关反应热的计算.
专题:
化学反应中的能量变化.
分析:
根据燃烧热写出热化学方程式,再利用盖斯定律来计算反应2C(s)+2H2(g)+O2(g)=CH3COOH(1)的反应热.
解答:
解:25℃、101kPa下,H2(g)、C(s)和CH3COOH(l)的燃烧热分别是285.8kJ•mol﹣1、393.5kJ•mol﹣1和870.3kJ•mol﹣1,
则H2(g)+ O2(g)=H2O(l)△H=﹣285.8kJ•mol﹣1①,
O2(g)=H2O(l)△H=﹣285.8kJ•mol﹣1①,
C(s)+O2(g)=CO2(g)△H=﹣393.5kJ•mol﹣1②,
CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H=﹣870.3kJ•mol﹣1③,
由盖斯定律可知,①×2+②×2﹣③可得反应2C(s)+2H2(g)+O2(g)=CH3COOH(1),
其反应热为2×(﹣285.8kJ•mol﹣1)+2×(﹣393.5kJ•mol﹣1)+870.3kJ•mol﹣1=﹣488.3KJ•mol﹣1,
故选A.
点评:
本题考查学生盖斯定律计算反应热的知识,可以根据所学知识进行回答,难度不大.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
下图是由常见元素组成的一些单质及其化合物之间的转化关系图。常温常压下,B、E、F、H、I均为气体,F为无色无味,且能使澄清石灰水变混浊;B、E、I均有刺激性气味,E能使湿润的红色石蕊试纸变蓝,B、E在空气中相遇会产生白烟,I为红棕色。A是一种常见的肥料。C、G、K的焰色反应呈黄色。(反应中生成的部分物质已略去)
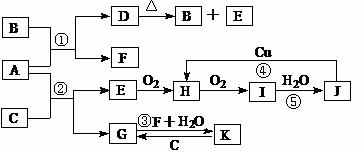
请回答下列问题:
(1)物质D的化学式为  ;
;
(2)写出反应③的化学方程式  ;
;
(3)写出反应④的离子方程式 ;
(4)写出反应⑤的化学方程式,并在方程式上标出电子转移的方向和数目 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列反应在水溶液中不可能发生的是( )
A.3Cl2+6FeI2=2FeCl3+ 4FeI3 B.Cl2+FeI2=FeCl2+I2
C.C o2O3+6HCl=2CoCl2+Cl2↑+3H2O
o2O3+6HCl=2CoCl2+Cl2↑+3H2O  D.2Fe3++2I-=2Fe2++I2
D.2Fe3++2I-=2Fe2++I2
查看答案和解析>>
科目:高中化学 来源: 题型:
利用芳香烃X和烯烃Y可以合成紫外线吸收剂BA D,其结构简式为:
D,其结构简式为:
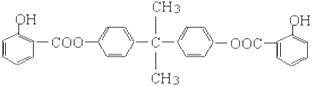
BAD的合成路线如下:
已知:G不能发生银镜反应,B遇FeCl3溶液显紫色,C到D的过程为引入羧基(—COOH)的反应。

试回答下列问题:
(1)写出结构简式:Y ,D 。
(2)上述属于取代反应的有 ( 填数字序号)。
(3)1molBAD最多可与含  molNaOH的溶液完全反应。
molNaOH的溶液完全反应。
(4)E有多种同分异构体,判断符合下列要求的同分异构体数目为 种。
①能发生银镜反应 ②遇FeCl3溶液显紫色 ③核磁共振氢谱图中有四个吸收峰
(5)写出反应②和④方程式 。
| |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于硝酸的说法正确的是( )
|
| A. | 硝酸与金属反应时,主要是+5价的氮得电子 |
|
| B. | 浓HNO3与浓HCl按3:1的体积比所得的混合物叫王水 |
|
| C. | 硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2 |
|
| D. | 常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )
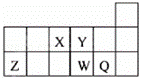
|
| A. | 元素X与元素Z的最高正化合价之和的数值等于8 |
|
| B. | 原子半径的大小顺序为:rX>rY>rZ>rW>rQ |
|
| C. | 离子Y2﹣和Z3+的核外电子数和电子层数都不相同 |
|
| D. | 元素W的最高价氧化物对应的水化物的酸性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
50mL 0.50mol•L﹣1的盐酸与50mL 0.55mol•L﹣1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热,完成下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 .请指出装置中的另外错误是 .
(2)烧杯间填满碎纸条的作用是 .
(3)大烧杯上如不盖硬纸板,求得的中和热 (填“偏大”“偏小”“无影响”).
(4)实验中改用60mL 0.50 mol•L﹣1的盐酸跟60mL 0.55 mol•L﹣1NaOH溶液进行上述实验相比,所放出的热量 (填“相等”“不相等”),所求中和热 (填“相等”“不相等”).
(5)用相同浓度体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会 ;用50mL 0.50mol•L﹣1NaOH溶液进行上述实验,测得的中和热的数值会 (均填“偏大”“偏小”“无影响”).

查看答案和解析>>
科目:高中化学 来源: 题型:
海水中有丰富的资源,多种多样的海洋动物和植物,海底有丰富的矿藏、石油、天然气等,此外,海水中还含有大量的电解质,它们电离产生Cl﹣、Br﹣(溴离子)、SO42﹣、Na+、Mg2+、Ca2+等,都是重要资源.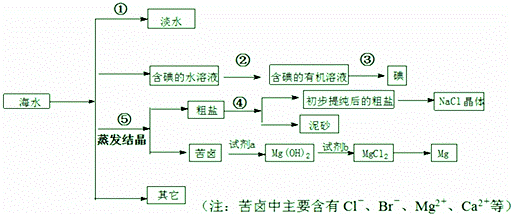
(1)写出步骤①、②、④分离提纯的方法:
① ② ④
(2)步骤②分离提纯过程中需要选用主要玻璃仪器的名称 .
(3)欲除去初步提纯后的粗盐中的MgCl2、CaCl2和Na2SO4,应向该粗食盐水中依次加入NaOH溶液、 溶液、 溶液,然后过滤;为尽可能除去杂质,每次加入的试剂应 量.向所得溶液中滴加 至无气泡产生,再经蒸发结晶得到食盐晶体.
(4)检验淡水中是否含有Cl﹣ 的操作现象及结论 .
(5)写出加入试剂a后,发生反应的离子方程式 .
(6)工业上用电解饱和食盐水的方法生产氯气、氢气和烧碱,请写出利用氯气和消石灰制取漂白粉的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是()
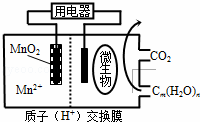
A. 分子组成为Cm(H2O)n的物质一定是糖类
B. 微生物所在电极区放电时发生还原反应
C. 放电过程中,H+从正极区移向负极区
D. 正极反应式为:MnO2+4H++2e﹣═Mn2++2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com