
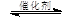 4NO(g)+CO2(g)+2H2O(g) △H1<0
4NO(g)+CO2(g)+2H2O(g) △H1<0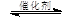 2N2(g)+CO2(g)+2H2O(g) △H2<0
2N2(g)+CO2(g)+2H2O(g) △H2<0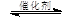 N2(g) +CO2(g) +2H2O(g) △H3= 。(用△H1和△H2表示)
N2(g) +CO2(g) +2H2O(g) △H3= 。(用△H1和△H2表示)| 投料比[n(NO2) / n(CH4)] | 400 K | 500 K | 600 K |
| 1 | 60% | 43% | 28% |
| 2 | 45% | 33% | 20% |
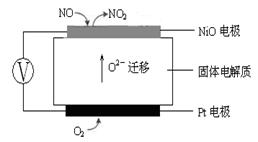

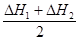 (1分)
(1分)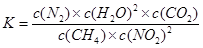 (1分) 不变 (2分)
(1分) 不变 (2分)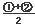 即为目标方程式③,所以,
即为目标方程式③,所以,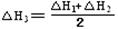
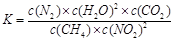
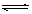 N2(g) + CO2(g) + 2H2O(g)
N2(g) + CO2(g) + 2H2O(g)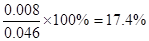
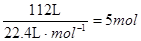 。
。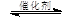 4NO(g) + CO2(g)+2H2O(g)
4NO(g) + CO2(g)+2H2O(g) 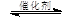 2N2(g) + CO2(g)+2H2O(g)
2N2(g) + CO2(g)+2H2O(g) 

 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO(g)+ H2(g);
CO(g)+ H2(g); CO (g)+ 3H2(g)
CO (g)+ 3H2(g)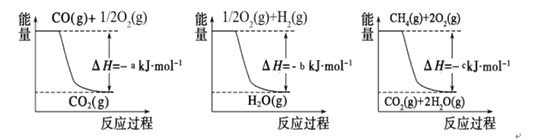
 2NH3(g),按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
2NH3(g),按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3 mol H2、2 mol N2 | 6 mol H2、4mol N2 | 2 mol NH3 |
| 达到平衡的时间(min) | t | 5 | 8 |
| 平衡时N2的浓度(mol·L-1) | c1 | 3 | |
| N2的体积分数 | ω1 | ω2 | ω3 |
| 混合气体密度(g·L-1) | ρ1 | ρ2 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2CO2(g)+ N2(g) △H<0,
2CO2(g)+ N2(g) △H<0,
 N2O4(g) ΔH=-56.9 kJ/mol ②
N2O4(g) ΔH=-56.9 kJ/mol ② 2N2(g) + 3H2O(g)。
2N2(g) + 3H2O(g)。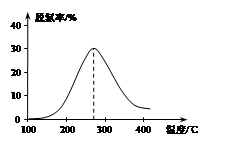

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g)ΔH=-92.2kJ·mol-1
2NH3(g)ΔH=-92.2kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ②镍氢电池的使用可以减少对环境的污染,它采用储氢金属为负极,碱液NaOH为电解液,镍氢电池充电时发生反应 。其放电时的正极的电极反应方程式为 。
②镍氢电池的使用可以减少对环境的污染,它采用储氢金属为负极,碱液NaOH为电解液,镍氢电池充电时发生反应 。其放电时的正极的电极反应方程式为 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 4PCl3(g) + a kJ, P4(s)+10Cl2(g)
4PCl3(g) + a kJ, P4(s)+10Cl2(g) 4PCl5(g) + b kJ。P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ/mol,PCl3中P-Cl键的键能为1.2c kJ/mol。下列叙述正确的是
4PCl5(g) + b kJ。P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ/mol,PCl3中P-Cl键的键能为1.2c kJ/mol。下列叙述正确的是| A.P-P键的键能大于P-Cl键的键能 |
B.可求Cl2(g)+PCl3(g) PCl5(s)的反应热 PCl5(s)的反应热 |
C.Cl-Cl键的键能为 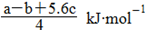 |
D.P-P键的键能为  |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。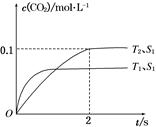

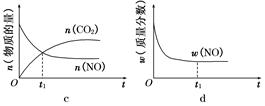
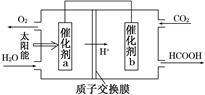
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.-252.9 kJ·mol-1 | B.+252.9 kJ·mol-1 |
| C.-604.5 kJ·mol-1 | D.+604.5 kJ·mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com