
| A. | 在标准状况下,2.24L 苯中含有 0.6NA个碳原子 | |
| B. | 1 L PH=l的硫酸溶液中含有0.2NA个氢离子 | |
| C. | 1 L 1 mol•L-1的 FeC13溶液中,含有铁离子的数目为NA | |
| D. | t℃时,1 L pH=6的纯水中,含有10-6NA个OH- |
分析 A、标况下,苯为液体;
B、氢离子的个数根据N=CVNA来计算;
C、铁离子是弱碱阳离子,在溶液中会水解;
D、根据纯水永远显中性来分析.
解答 解:A、标况下,苯为液体,故不能根据气体摩尔体积来计算,故A错误;
B、pH=1的硫酸溶液中c(H+)=0.1mol/L,故氢离子的个数根据N=CVNA=0.1mol/L×1L×NA=0.1NA个,故B错误;
C、铁离子是弱碱阳离子,在溶液中会水解,故溶液中的铁离子的个数小于NA个,故C错误;
D、无论在什么温度下,纯水永远显中性,则1 L pH=6的纯水中,氢离子的浓度为10-6mol/L,则氢氧根的浓度也为10-6mol/L,故含有氢氧根的个数N=CVNA=10-6NA,故D正确.
故选D.
点评 本题考查了物质的量的有关计算,根据物质的结构和公式来分析计算是解题关键,难度不大.


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:填空题
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为ADF |
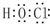 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池放电时,溶液中的阳离子移向正极 | |
| B. | 电池放电时,H2是正极 | |
| C. | 电池充电时,氢元素被氧化 | |
| D. | 电池放电时,电池负极周围溶液的pH不断增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
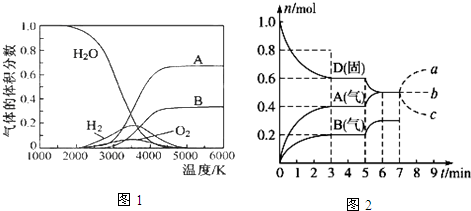
| 压强(KPa) | 200 | 500 | 1000 |
| B的浓度(mol/L) | 0.04 | 0.1 | 0.27 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜片投入足量稀硝酸中:Cu+NO3-+4H+═Cu2++NO↑+2H2O | |
| B. | 二氧化硅与氢氧化钠溶液反应:SiO2+2OH-═SiO32-+H2O | |
| C. | 硫酸溶液与氢氧化钡溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 钠与 CuSO4溶液反应:2Na+Cu2+═2Na++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和盐酸:Fe+2H+═Fe3++H2↑ | |
| B. | 石灰石和硝酸:CO32-+2H+═H2O+CO2↑ | |
| C. | 铜和硝酸银溶液:Cu+Ag+═Cu2++Ag | |
| D. | 氢氧化钡溶液和硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去水瓶中的水垢:CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O | |
| B. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| C. | 用稀氢氧化钠溶液吸收二氧化氮:2OH-+2NO2═NO3-+NO↑+H2O | |
| D. | 等物质的量的Ba(OH)2与(NH4)2Fe(SO4)2在溶液中反应:Ba2++2OH-+2NH4++SO42-═BaSO4↓+2NH3•H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com