
【题目】【2017届江苏省海安高级中学高三月考】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
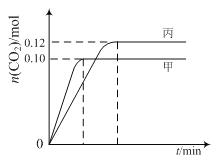
各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
容器 | 温度/℃ | 起始物质的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
下列说法正确的是
A.该反应的正反应为吸热反应
B.达到平衡时,乙中CO2的体积分数比甲中的小
C.T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)>v(逆)
D.T2℃时,若起始时向丙中充入0.06mol N2和0.12 mol CO2,则达平衡时N2的转化率大于40%
【答案】CD
【解析】
试题分析:A.2NO(g)+2CO(g)N2(g)+2CO2(g),先拐先平温度高,甲状态温度高于丙,T1>T2,此时甲平衡状态二氧化碳物质的量小,说明温度越高平衡逆向进行,逆反应为吸热反应,正反应为放热反应,故A错误;
B.乙中可以看做是甲起始量达到平衡状态,再加入0.1molNO和0.1molCO,相当于增大平衡压强,平衡正向进行,达到平衡时,乙中CO2的体积分数比甲中的大,故B错误;
C.甲状态下平衡时CO物质的量为0.10mol,结合三行计算计算平衡常数,
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始量(mol/L) 0.1 0.1 0 0
变化量(mol/L) 0.05 0.05 0.025 0.05
平衡量(mol/L) 0.05 0.05 0.025 0.05
K=![]() =10,
=10,
T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,Qc=![]() =2.5<K=10.则反应达到新平衡前v(正)>v(逆),故C正确;
=2.5<K=10.则反应达到新平衡前v(正)>v(逆),故C正确;
D.T2℃时,平衡状态CO物质的量为0.12mol,
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始量(mol) 0.2 0.2 0 0
转化量(mol) 0 0 0.1 0.2
变化量(mol) 0.08 0.08 0.04 0.08
平衡量(mol) 0.12 0.12 0.04 0.08
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始量(mol) 0 0 0.06 0.12
转化量 0.12 0.12 0 0
若起始时向丙中充入0.06mol N2和0.12 mol CO2,反应逆向进行得到平衡状态,和起始量为0.12molNO和0.12molCO达到的平衡相同,和起始量0.2molCO、NO相比,相当于减少了NO、CO0.08mol的CO、NO,压强减小平衡逆向进行,所以氮气转化率大于40%,故D正确;故选CD。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是、
A. 在一定温度和压强下,各种气态物质体积大小由构成气体分子大小决定
B. 在一定温度和压强下,各种气态物质体积的大小由构成气体的分子数决定
C. 不同的气体,若体积不同,则它们所含的分子数—定不同
D. 气体摩尔体积是指1mol任何气体所占的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铁片与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率,可以使用如下方法中的(选填序号). ①加20mL蒸馏水 ②升高温度(不考虑盐酸挥发)③加NaCl溶液 ④滴入几滴硫酸铜溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 18g重水(D2O)所含的电子数为10NA
B. 常温常压下,0.3molNO2完全与水反应,转移的电子数为0.2NA
C. 标准状况下,22.4LCCl4中含有NA个CCl4分子
D. 常温下, 1L0.1mol/LCH3COONH4溶液中NH4+离子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有以下一系列反应,最终产物为乙二酸。

试回答下列问题:
(1)C的结构简式是______________。
B→C的反应类型是________________,
E→F的化学方程式是___________________。
(2)E与乙二酸发生酯化反应生成环状化合物的化学方程式是__________________。
(3)由B发生水解反应或C与H2O发生加成反应均生成化合物G。在乙二酸、水、苯酚、G四种分子中,羟基上氢原子的活泼性由强到弱的顺序是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2015福建理综、12】在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列判断不正确的是( )

A.a=6.00
B.同时改变反应温度和蔗糖的浓度,v可能不变
C.b<318.2
D.不同温度时,蔗糖浓度减少一半所需的时间相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铝土矿为原料,提取氧化铝,冶炼铝的工艺流程如下,下列说法错误的是
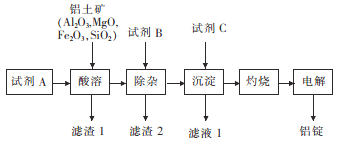
已知:滤渣2主要成分是氢氧化铁、氢氧化镁,B的焰色呈黄色。
A. 试剂A可以是稀硫酸或盐酸 B. 加入试剂B除去Mg2+、Fe3+
C. 滤渣1主要成分是SiO2 D. 电解氧化铝时在阴极上定期补炭块
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国现阶段的能源结构仍以化石能源为主,为减少化石能源消耗、实现可持续发展,我国提出了“构建节约型社会”的口号。下列节约化石能源的措施不切实际的是
A. 充分利用太阳能 B. 充分利用风力和水力发电
C. 提高能源利用率 D. 不使用含碳的能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,针对表中的①—⑧八种元素,用元素符号或化学式回答相关问题:

(l)在这些元素中,化学性质最不活泼原子的原子结构示意图为______.
(2)用电子式表示①与③形成化合物的过程______.:
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是______. ,②、④的最高价氧化物对应水化物的溶液反应的离子方程式为:______.
(4)①②③④四种元素的简单离子半径由大到小的顺序是______.(用离子符号和“>”表示)。
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是______.(用化学式和“>”表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com