
| A. | 除去Cl2中少量HC1气体:通过饱和食盐水后再干燥气体 | |
| B. | 除去Na2CO3固体中少量NaHCO3:置于坩埚中加热 | |
| C. | 除去Fe(OH)3胶体中溶有的少量NaCl:加入适量水后过滤 | |
| D. | 除去CuCl2溶液中少量的FeCl3:加入稍过量的CuO后过滤 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Fe2+、Na+、H+、SO42- | B. | H+、Ba2+、Cl-、NO3- | ||
| C. | Ba2+、Na+、OH-、SO42- | D. | Na+、Mg2+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn、Al | B. | Fe、Zn | C. | Al、Mg | D. | Mg、Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
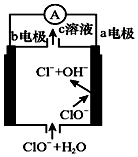
| A. | 电池工作时,c溶液中的溶质一定是MgCl2 | |
| B. | 负极反应式:ClO--2e-+H2O=Cl-+2OH- | |
| C. | 电池工作时,OH-向b电极移动 | |
| D. | b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业合成氨时使用催化剂 | |
| B. | 配制SnCl2溶液时加入一定量的盐酸 | |
| C. | 25℃时,在稀硫酸溶液中由水电离出的c(H+)<1×10-7mol/L | |
| D. | AgCl在水中的溶解度大于在饱和NaCl溶液中的溶解度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在镀件上电镀铜时,可用金属铜作阳极 | |
| B. | 镀层破损后,白铁(镀锌)比马口铁(镀锡)更易被腐蚀 | |
| C. | 工业上电解饱和食盐水制烧碱,NaOH在阴极产生 | |
| D. | 钢铁在发生析氢腐蚀和吸氧腐蚀时,完全相同的反应是负极反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 起始加入量(mol) | 平衡时 | ||||
| A | B | C | A或C转化率(%) | C的物质的量分数(%) | 放出或吸收热量(KJ) |
| 1 | 1 | 0 | α1 | φ1 | Q1 |
| 0 | 0 | 2 | α2 | φ2 | Q2 |
| 2 | 2 | 0 | α2 | φ3 | Q3 |
| A. | α1+α2=1;φ2=φ1 | B. | φ3=2φ1;Q3=2Q1 | C. | φ3=φ1=φ2;Q3=2Q1 | D. | α1=α3;Q1+Q2=Q |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每当固体质量减轻5.6g时,生成2.8g Si | |
| B. | 氧化剂和还原剂的物质的量之比为1:2 | |
| C. | 硅单质在常温下不与任何酸、碱反应 | |
| D. | 单质硅与单质碳均具有一定的还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com