
【题目】下列物质属于有机物的是 ( )
A. 氰化钾(KCN) B. 氰酸铵(NH4CNO)
C. 尿素(NH2CONH2) D. 碳化硅(SiC)
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)请用系统命名法给下列有机物予以命名:
① ________________ ②
________________ ② ___________________
___________________
(2)相对分子质量为72且沸点最低的烷烃的结构简式____________
(3)与H2加成生成2,5﹣二甲基己烷的炔烃的系统命名_________________
(4)![]() 的系统命名__________________________.
的系统命名__________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1 mol任何物质都含有6.02×1023个分子
B.标准状况下,1 mol H2和1 mol H2O所占的体积都约为22.4 L
C.HNO3的摩尔质量是63 g
D.0.5 mol 13H原子含有的中子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下的恒容密闭容器中,反应A2(g)+B2(g)![]() 2AB(g)达到平衡的标志是
2AB(g)达到平衡的标志是
A. 每断裂1molA-A键,同时也断裂1molB-B键
B. 浓度之比c(A2): c(B2): c(AB)=1:1:2
C. 各物质的浓度不再改变
D. 当混合物的密度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素镓和砷的单质及其化合物在工业生产上有重要的用途。回答下列问题:
(1)砷元素基态原子的电子排布式为_______________________。
(2)砷与氢元素可形成化合物砷化氢,该化合物的空间构型为_____________,其中砷原子的杂化方式为__________。
(3)根据等电子原理,写出由短周期元素组成且与砷化氢互为等电子体的一种离子的化学式________。
(4)已知由元素砷与镓元素组成的化合物A为第三代半导体。已知化合物A的晶胞结构与金刚石相似,其中砷原子位于立方体内,镓原子位于立方体顶点和面心,请写出化合物A的化学式____________;
(5)已知铝与镓元素位于同一主族,金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm-3,通过计算确定铝原子在三维空间中堆积方式________________(已知NA=6.02×1023,1pm=10-10cm,4053=6.64×107);晶胞中距离最近的铝原子可看作是接触的,列式计算铝的原子半径r(A1)=______pm.(只列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定条件下,体积为2L的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0 mol和6.0 mol,3min后达到平衡,生成NH3的物质的量是2.4 mol。试求:
2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0 mol和6.0 mol,3min后达到平衡,生成NH3的物质的量是2.4 mol。试求:
① 3min内用N2表示的化学反应速率为____________。②H2的转化率是____________。
(2)某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
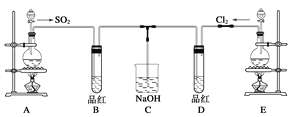
a.实验室用装置E制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子物质的量为____________;
MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子物质的量为____________;
b.①反应开始一段时间后,观察到D试管中的品红溶液出现的现象是:
D:_____________________________________________________________。
②停止通气后,再给B、D两个试管分别加热;两个试管中的现象分别为:
B:____________________________________,D:________________________________。
c.另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z、T四种短周期元素。X、Y、Z三元素在周期表中的位置如图所示,三元素的原子序数之和是41。X和T的单质在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄色固体)常见的两种化合物。
X | |
Y | Z |
(1)各元素的符号是X______,Y________,Z________、T___________。
(2)Y原子的结构示意图为______________________________________________。
(3)用电子式表示Y与T组成的化合物的形成过程:_____________________。
(4)X和Y的氢化物的稳定性_________(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于漂白粉的叙述正确的是( )
A.漂白粉的有效成分是Ca(ClO)2和CaCl2
B.漂白粉在空气中久置后会变质
C.漂白粉是由Cl2与烧碱制得的
D.在使用漂白粉时应用浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸工业尾气中的NO、NO2进入大气后,会形成光化学烟雾、破坏臭氧层等。可用氢氧化钠溶液对含氮氧化物的废气进行处理,反应的化学方程式如下:
NO2+NO+2NaOH=2 NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
氨气也可以用来处理氮氧化物。例如,氨气与一氧化氮可发生如下反应: 4NH3+6NO=5N2+6H2O
将一定量NO和NO2的混合气体通入300 mL 5mol/LNaOH溶液中,恰好被完全吸收。下列说法不正确的
A. 原混合气体中NO在标准状况下的体积可能为16.8 L
B. 所得溶液中NaNO3和NaNO2的物质的量之比可能为1︰2
C. 若用氨气处理,所需氨气在标准状况下的体积可能为22.4 L
D. 在用氨气处理氮氧化物时,氮氧化物发生还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com