
【题目】非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用CsCO3,XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7,的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为__;第一电离能I1(Si)__I1(Ge)(填![]() 或
或![]() )。
)。
(2)基态Ge原子核外电子排布式为__;SiO2,GeO2具有类似的晶体结构,其中熔点较高的是__,原因是__。
(3)如图为H3BO3晶体的片层结构,其中B的杂化方式为__;硼酸在热水中比在冷水中溶解度显著增大的主要原因是__。

(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7,属正交晶系(长方体形),晶胞参数为apm、bpm和cpm。如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为__;CsSiB3O7的摩尔质量为Mg·mol-1,设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为__g·cm-3(用代数式表示)。

【答案】O>C>Si > 1s22s22p63s23p63d104s24p2(或[Ar]3d104s24p2) SiO2 二者均为原子晶体,Ge原子半径大于Si,Si-O键长小于Ge-O键长,SiO2键能更大,熔点更高 sp2 热水破坏了硼酸晶体中的氢键,并且硼酸分子与水形成分子间氢键,使溶解度增大 4 ![]()
【解析】
⑴电负性的变化规律为同周期从左向右逐渐增大,同主族由上至下逐渐减小,第一电离能的变化规律为同族元素由上至下逐渐减小。
⑵SiO2、GeO2为同类型晶体结构,即为原子晶体,Ge原子半径大于Si,Si-O键长小于Ge-O键长,SiO2键能更大,熔点更高。
⑶B原子最外层有3个电子,与3个-OH形成3个共价键,即可得杂化方式,热水破坏了硼酸晶体中的氢键,并且硼酸分子与水形成分子间氢键,使溶解度增大。
⑷先分析得出Cs的个数,再根据公式计算密度。
⑴电负性的变化规律为同周期从左向右逐渐增大,同主族由上至下逐渐减小,所以电负性O>C>Si;第一电离能的变化规律为同族元素由上至下逐渐减小,因此I1(Si)>I1(Ge),故答案为:O>C>Si;>。
⑵Ge原子位于第四周期IVA族,因此原子核外电子排布式为1s22s22p63s23p63d104s24p2(或[Ar]3d104s24p2);SiO2、GeO2均为原子晶体,Ge原子半径大于Si,Si-O键长小于Ge-O键长,SiO2键能更大,熔点更高,故答案为:1s22s22p63s23p63d104s24p2(或[Ar]3d104s24p2);SiO2;Ge原子半径大于Si,Si-O键长小于Ge-O键长,SiO2键能更大,熔点更高。
⑶B原子最外层有3个电子,与3个-OH形成3个共价键,因此为sp2杂化;热水破坏了硼酸晶体中的氢键,并且硼酸分子与水形成分子间氢键,使溶解度增大;故答案为:p2;热水破坏了硼酸晶体中的氢键,并且硼酸分子与水形成分子间氢键,使溶解度增大。
⑷原子分数坐标为(0.5,0.2,0.5)的Cs原子位于晶胞体内,原子分数坐标为(0,0.3,0.5)及(1.0,0.3,0.5)的Cs原子位于晶胞的yz面上,原子分数坐标为(0.5,0.8,1.0)及(0.5,0.8,0)的Cs原子位于晶胞xy面上,原子分数坐标为(0,0.7,1.0)及(1.0,0.7,1.0)(0,0.7,0)及(1.0,0.7,0)的Cs原子位于晶胞平行于y轴的棱上,利用均摊法可计算该晶胞中共含Cs原子4个;带入晶胞密度求算公式可得:
ρ=![]() g·cm-3,故答案为:4;
g·cm-3,故答案为:4;![]() 。
。


科目:高中化学 来源: 题型:
【题目】晶体硅是一种重要的非金属材料,有科学家认为硅是“21世纪的能源”、“未来的石油”。
(1)工业上生产纯硅的工艺流程如下:
![]()
石英砂的主要成分是SiO2,在制备粗硅时,焦炭的作用是__________(填“氧化剂”或“还原剂”);在该反应中,若消耗了3.0 g SiO2 ,则转移电子的总数为_______________。
(2)某实验室利用SiHCl3(沸点33.0 ℃)与过量H2在1 000 ℃~1 100 ℃反应制得纯硅。已知SiHCl3能与H2O强烈反应,在空气中易自燃。装置如图所示(热源及夹持装置略去)。
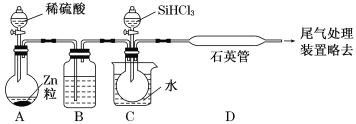
①装置B中的试剂是___________。装置C中的烧瓶需要加热,其目的是_________________。
②反应一段时间后,装置D中观察到的现象是______________________;装置D中发生反应的化学方程式为___________________________________。
③为检验产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需要加入的试剂有______(填字母)。
a.碘水 b.氯水 c.Na2SO3溶液 d.KSCN溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
晶体硼(其每个结构单元中有12个B原子) | NaCl | S8 | HCN | |
结构模型示意图 |
|
|
|
|
备注 | 熔点2573K | —— | 易溶于CS2 | —— |
A.晶体硼属于原子晶体,结构单元中含有30个B-B键,含20个正三角形
B.NaCl晶体中每个Na+周围距离最近且相等的Na+有6个
C.S8分子中的共价键为非极性键
D.HCN分子中含有2个σ键,2个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C为电子层数小于或等于3的元素,A元素原子M层电子数为K层电子数的![]() ,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的
,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的![]() 。由此推断三种元素原子的核电荷数及元素名称分别是A__________;B________;C________。
。由此推断三种元素原子的核电荷数及元素名称分别是A__________;B________;C________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中含有的哑铃形C22-的存在,使晶胞沿一个方向拉长(该晶胞为长方体)。下列关于CaC2晶体的说法中正确的是( )
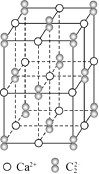
A.1个Ca2+周围距离最近且等距离的C22-数目为6
B.6.4gCaC2晶体中含阴离子0.1mol
C.该晶体中存在离子键和共价键
D.与每个Ca2+距离相等且最近的Ca2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温下的六种溶液:①0.01mol·L-1CH3COOH溶液;②0.01mol·L-1HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液;⑤0.01mol·L-1CH3COOH溶液与pH=12的氨水等体积混合后所得溶液;⑥0.01mol·L-1HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)将②③混合后所得溶液pH=7,则消耗溶液的体积:②__(填“>”“<”或“=”)③。
(2)若将②③等体积混合后,则所得混合溶液中各离子浓度大小顺序为__。
(3)将六种溶液稀释100倍后,比较溶液的pH:③__(填“>”“<”或“=”)④。
(4)水的电离程度相同的是__(填序号)。
(5)将①④混合,若有c(CH3COO-)>c(Na+),则混合液呈_(填字母)。
A.酸性 B.碱性 C.中性 D.三性皆有可能
(6)若改变温度后,测得④溶液pH=10,则该温度下Kw=__。在该温度下,将①④混合后,测得溶液pH=7,则所得溶液中c(Na+)-c(CH3COO-)=__mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种兴奋剂的结构简式如图: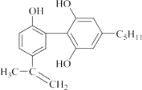 ,下列有关该物质的说法正确的是( )。
,下列有关该物质的说法正确的是( )。
A.1mol 该物质与浓溴水和H2 反应时,最多消耗 Br2 和H2 的物质的量分别为 4 mol、7 mol
B.该分子中所有碳原子可以稳定的共存在一个平面中
C.遇 FeCl3 溶液显紫色,因为该物质与苯酚属于同系物
D.滴入酸性 KMnO4 溶液,观察到紫色褪去,可证明分子中存在双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。利用下图所示的装置进行实验,实验进行时试管A中应加入的试剂是__________;烧瓶B的作用是________;烧瓶C的作用是________;用点燃的木条靠近水槽中的肥皂泡时的现象是_______________。
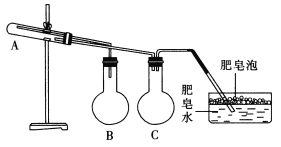
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某天然碱可看作由CO2和NaOH反应后的产物所组成。为了确定其组成,现称取天然碱3.32g,做如下实验:(气体均折算为标准状况下)

(1)B的电子式_______。
(2)天然碱受热分解的反应方程式______。
(3)过量的天然碱溶液滴加少量的Ba(OH)2溶液,请写出离子反应方程式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com