
【题目】氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,易溶于水,难溶于CCl4,某研究小组用如图1所示的实验装置制备氨基甲酸铵。
反应原理:2NH3(g)+CO2(g)![]() NH2COONH4(s) △H<0。
NH2COONH4(s) △H<0。

(1)仪器2的名称是__。仪器3中NaOH固体的作用是__。
(2)①打开阀门K,仪器4中由固体药品所产生的气体就立即进入仪器5,则该固体药品的名称为__。
②仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内稀硫酸溶液中产生气泡,应该__(填“加快”、“减慢”或“不改变”)产生氨气的流速。
(3)另有一种制备氨基甲酸铵的反应器(CCl4充当惰性介质)如图2:

①图2装置采用冰水浴的原因为__。
②当CCl4液体中产生较多晶体悬浮物时,即停止反应,__(填操作名称)得到粗产品。
为了将所得粗产品干燥可采取的方法是__。
A.蒸馏 B.高压加热烘干 C.真空微热烘干
(4)①已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式为__。
②为测定某样品中氨基甲酸铵的质量分数,某研究小组用该样品进行实验。已知杂质不参与反应,请补充完整测定某样品中氨基甲酸铵质量分数的实验方案:用天平称取一定质量的样品,加水溶解,__,测量的数据取平均值进行计算(限选试剂:蒸馏水、澄清石灰水、Ba(OH)2溶液)。
【答案】三颈烧瓶 干燥氨气,防止生成的氨基甲酸铵水解 干冰 加快 降低温度,有利于提高反应物的转化率,防止因反应放热造成NH2COONH4分解 过滤 C NH2COONH4+2H2O=NH4HCO3+NH3H2O或NH2COONH4+H2O=NH4HCO3+NH3↑ 加入足量氢氧化钡溶液,充分反应后,过滤、用蒸馏水洗涤所得沉淀、干燥后称量沉淀的质量,重复2~3次
【解析】
根据装置:仪器2制备氨气,由于氨基甲酸铵易水解,所以用仪器3干燥氨气,利用仪器4制备干燥的二氧化碳气体,在仪器5中发生2NH3(g)+CO2(g)NH2COONH4(s)制备氨基甲酸铵;
(1)根据仪器构造可得;考虑氨基甲酸铵水解;
(2)①仪器4制备干燥的二氧化碳气体,为干冰;
②反应初期观察到装置内稀硫酸溶液中产生气泡,说明二氧化碳过量,氨气不足;
(3)①考虑温度对反应的影响和氨基甲酸铵受热分解;
②过滤得到产品,氨基甲酸铵易分解,所得粗产品干燥可真空微热烘干;
(4)①氨基甲酸铵可完全水解为碳酸氢铵和一水合氨,据此书写;
②测定某样品中氨基甲酸铵的质量分数,可以使其水解得到NH4HCO3,用氢氧化钡沉淀得到碳酸钡沉淀,通过碳酸钡的质量可得氨基甲酸铵的质量,进而可得其质量分数,据此可得。
(1)根据图示,仪器2的名称三颈烧瓶;仪器3中NaOH固体的作用是干燥氨气,防止生成的氨基甲酸铵水解;故答案为:三颈烧瓶;干燥氨气,防止生成的氨基甲酸铵水解;
(2)①反应需要氨气和二氧化碳,仪器2制备氨气,仪器4制备干燥的二氧化碳气体,立即产生干燥的二氧化碳气体,则为干冰;故答案为:干冰;
②氨气易溶于稀硫酸,二氧化碳难溶于稀硫酸,若反应初期观察到装置内稀硫酸溶液中产生气泡,说明二氧化碳过量,应该加快产生氨气的流速;故答案为:加快;
(3)①该反应为放热反应,温度升高不利于合成,故采用冰水浴可以降低温度,有利于提高反应物的转化率,防止因反应放热造成H2NCOONH4分解;故答案为:降低温度,有利于提高反应物的转化率,防止因反应放热造成H2NCOONH4分解;
②当CCl4液体中产生较多晶体悬浮物时,即停止反应,过滤,为防止H2NCOONH4分解,真空微热烘干粗产品;故答案为:过滤;C;
(4)①氨基甲酸铵可完全水解为碳酸氢铵,反应为:NH2COONH4+2H2O=NH4HCO3+NH3H2O或NH2COONH4+H2O=NH4HCO3+NH3↑;故答案为:NH2COONH4+2H2O=NH4HCO3+NH3H2O或NH2COONH4+H2O=NH4HCO3+NH3↑;
②测定某样品中氨基甲酸铵的质量分数,可以使其水解得到NH4HCO3,用氢氧化钡沉淀得到碳酸钡沉淀,通过碳酸钡的质量可得氨基甲酸铵的质量,进而可得其质量分数,具体方法为:用天平称取一定质量的样品,加水溶解,加入足量氢氧化钡溶液,充分反应后,过滤、用蒸馏水洗涤所得沉淀、干燥后称量沉淀的质量,重复2~3次,测量的数据取平均值进行计算;故答案为:加入足量氢氧化钡溶液,充分反应后,过滤、用蒸馏水洗涤所得沉淀、干燥后称量沉淀的质量,重复2~3次。


科目:高中化学 来源: 题型:
【题目】盐酸氨溴索(H)对于治疗老年重症肺炎有良好的疗效,其合成路线如下(部分反应条件及产物已略):
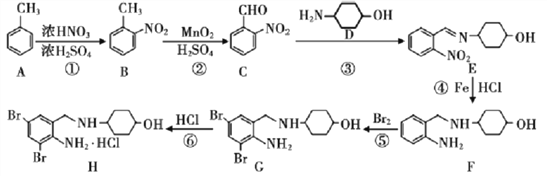
(1)B的名称为_________;反应①-⑥中为取代反应的是___________(填序号)。
(2)B的芳香族同分异构体J满足下列条件:
①可水解 ②可发生银镜反应 ③1mol J最多消耗2mol NaOH
J有________种;B的另一种芳香族同分异构体可与NaHCO3溶液反应,并有气体生成,其核磁共振氢谱有4组吸收峰,则它的结构简式为____________。
(3)可用碱性新制氢氧化铜悬浊液检验C中的特征官能团,写出该检验的离子反应方程式:____________________________。
(4)关于E的说法正确的是_________。
A.E难溶于水 B.E可使酸性KMnO4溶液褪色
C.1molE最多与1molH2加成 D.E不能与金属钠反应
(5)邻氨基苯甲酸甲酯(L)具有塔花的甜香味,也是合成糖精的中间体,以甲苯和甲醇为原料,无机试剂自选,参照H的合成路线图,设计L的合成路线____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法正确的是
A.18 g 18O含有的中子数为8NA
B.0.1 mol H2C2O4被氧化为CO2转移的电子数为0.1NA
C.标准状况下,a L氧气和氮气的脱合物中含有的原子总数约为![]() NA
NA
D.常温下、含1 mol H2SO4的浓硫酸与足量铜反应,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下:

为了研究X的结构,将化合物A在一定条件下水解只得到 和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。

(ⅰ)写出有机物的结构简式:D:______________,C:________________,E:______________。
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)
反应①__________________________________;反应⑥_____________________________。
(ⅲ)变化过程中的②属于____________反应,⑦属于________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对滴有酚酞试液的下列溶液,操作后颜色变深的是
A. 明矾溶液加热 B. CH3COONa溶液加热
C. 氨水中加入少量NH4Cl固体 D. 小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雌黄(As2S3)在我国古代常用作书写涂改修正液。浓硝酸氧化雌黄可制得硫磺,并生成砷酸和一种红棕色气体,利用此反应原理设计为原电池。下列叙述正确的是( )
A.砷酸的分子式为H2AsO4
B.红棕色气体在该原电池的负极区生成并逸出
C.该反应的氧化剂和还原剂物质的量之比为10:1
D.该反应中每析出4.8g硫磺转移1mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将盐酸滴加到Na2X溶液中,混合溶液的pOH[pOH=—lgc(OH-)]与离子浓度变化的关系如图所示。

下列叙述正确的是
A. 曲线N表示pOH与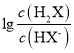 两者的变化关系
两者的变化关系
B. NaHX溶液中c(X2-)>c(H2X)
C. 当混合溶液呈中性时,c(Na+)=c(HX-)+2c(X2-)
D. 常温下,Na2X的第一步水解常数Kh1=1.0×10-4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2mol金属钠和1mol氯气反应的能量关系如图所示,下列说法不正确的是( )
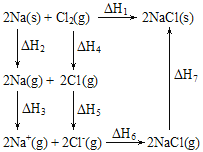
A.ΔH1=ΔH2+ΔH3+ΔH4+ΔH5+ΔH6+ΔH7
B.ΔH4的值数值上和Cl-Cl共价键的键能相等
C.ΔH7<0,且该过程形成了分子间作用力
D.ΔH5<0,在相同条件下,2Br(g)的ΔH5′>ΔH5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com