
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
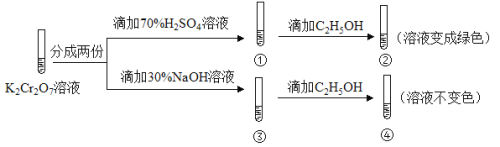
结合实验,下列说法不正确的是
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr2O72-被C2H5OH还原
C.对比②和④可知K2Cr2O7酸性溶液氧化性强
D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )。
A.CH2Cl2有 两种结构
两种结构
B.烯烃跟氢气起加成反应产物是2,2,3,4-四甲基戊烷,则这样的烯烃有3种
C. 的一氯代物有5种
的一氯代物有5种
D.1 mol某烷烃完全燃烧消耗11 mol O2,则其主链上含有5个碳原子的同分异构体(不考虑空间异构)有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、氧、磷、铁是与生命活动密切相关的元素。回答下列问题:
(1)P的基态原子最外电子层具有的原子轨道数为 ,Fe3+比Fe2+稳定的原因是 。
(2)N、O、P三种元素第一电离能最大的是 ,电负性最大的是 。
(3)含氮化合物NH4SCN溶液是检验Fe3+的常用试剂,SCN-中C原子的杂化类型为 ,1mol SCN-中含π键的数目为 NA。
(4)某直链多磷酸钠的阴离子呈如图所示的无极单链状结构,其中磷氧四面体通过共有顶角氧原子相连,则该多磷酸钠的化学式为 。
![]()
(5)FeO、NiO的晶体结构均与氯化钠晶体结构相同、其中Fe2+和Ni2+的离子半径分别为7.8×10-2nm、6.9×10-2nm,则熔点FeO NiO(填“<”、“>”或“=”)原因是 。
(6)磷化硼是一种超硬耐磨的涂层材料,其晶胞结构如图所示。P原子与B原子的最近距离为acm,则磷化硼晶胞的边长为 cm。(用含a的代数式表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均是短周期元素,A和B同周期, B和C同族,A元素族序数是周期数的三倍,B原子最外层电子数是内层电子数的二倍,B与A能生成化合物BA2,C与A生成化合物CA2, A的阴离子与D的阳离子电子层结构相同,都与氖原子的电子层结构相同,D 的单质与A 的单质在不同条件下反应,可生成D2A或D2A2。请回答
(1)写出元素符号B:_________ C:_________
(2)BA2的电子式 _________ ,BA2分子中化学键属于_________ 键。
(3)D2A2的化学式 _________ ,灼烧这化合物火焰呈_________ 色。
(4)C在元素周期表中的位置是第_________周期,_______族,其原子结构示意图为________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ:下列各项分别与哪个影响化学反应速率因素的关系最为密切?
(1)夏天的食品易变霉,在冬天不易发生该现象 ;
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢 ;
(3)MnO2加入双氧水中放出气泡更快 .
Ⅱ:在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
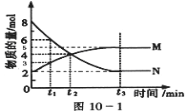
(1)比较t2时刻,正逆反应速率大小V正 V逆.(填“>”、“=”、“<”)
(2)若t2=2min,计算反应开始至t2时刻用M的浓度变化表示的平均反应速率为: .
(3)t3时刻化学反应达到平衡,反应物的转化率为 .
(4)如果升高温度,则V逆 (填增大、减小或不变).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 2 L 容积不变的密闭容器内,800 ℃时反应 2NO(g)+O2 (g)![]() 2NO2 (g)体系中,n(NO)随时间的变化如下表:
2NO2 (g)体系中,n(NO)随时间的变化如下表:

(1)用O2的反应速率表示 0~2s 内该反应的平均反应速率 v=________________。若上述反应在850 ℃下进行,反应2s时 n(NO)=0.009 mol,并且不再随时间而改变,则该反应是__________热反应。

(2)图中表示NO2浓度变化的曲线是__________(填字母)。
(3)能说明该反应已达到平衡状态的是________(填序号)。
A.v(NO2)=2v(O2)
B.容器内的压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内气体密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________(填序号)。
A.及时分离出NO2
B.适当升高温度
C.增大O2的浓度
D.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——化学与技术】过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。实验室可用工业碳酸钙(含MgCO3、FeCO3等杂质)制取纯净的碳酸钙,然后再用纯的碳酸钙制取过氧化钙,其主要流程如下:
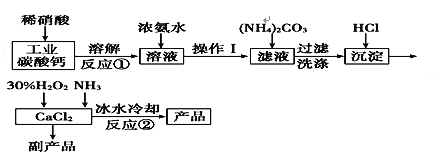
已知:CaO2·8H2O呈白色微溶于水,加热至350℃左右开始分解放出氧气,425℃分解完全。
(1)写出反应①中氧化还原反应的离子方程式:___________________________。
(2)向反应①后的溶液中加浓氨水的目的是:___________,________(用方程式表示)
(3)反应②常用冰水控制温度在0℃左右,其可能原因是(写出两种):
①__________________________;②__________________________。
(4)测定产品中CaO2的含量的实验步骤是
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol/L的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。已知:I2+2S2O===2I-+S4O。
某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能________(填“不受影响”“偏低”或“偏高”),原因是____________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示298K时N2与H2反应过程中的能量变化。根据右图叙述正确的是
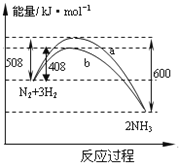
A.该反应的热化学方程式为:1/2N2(g)+3/2H2(g)![]() NH3(g) △H=-92kJ·mol-1
NH3(g) △H=-92kJ·mol-1
B.不用催化剂,生成 1molNH3放出的热量为46 KJ
C.加入催化剂,生成 1molNH3的反应热减小50 KJ·mol-1
D.曲线b表明加入催化剂降低了反应热,加快了反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,固定体积的密闭容器内,反应2HI(g)![]() H2 (g)+ I2 (g)达到平衡状态的标志是:
H2 (g)+ I2 (g)达到平衡状态的标志是:
①I2的体积分数不再变化;
②生成1 mol H2同时消耗1 molI2;
③容器内压强不再变化;
④生成2 mol HI同时消耗1molH2;
⑤气体的密度不再变化;
⑥混合气体的平均分子质量不再变化
A.①②③④⑤⑥ B.①②③⑤⑥ C.①②⑤⑥ D.①②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com