
【题目】mol/L是哪个物理量的单位( )
A. 物质的量 B. 摩尔质量 C. 气体摩尔体积 D. 物质的量浓度
科目:高中化学 来源: 题型:
【题目】(5分)短周期元素X、Y、Z、W核电荷数依次增大,X、Z同主族,Z、W同周期,四种元素的原子序数之和为37,在周期表中X是原子半径最小的元素,Y的最外层电子数是内层电子数的3倍。
(1)W在周期表中的位置是 。
(2)X与Y 能形成具有18个电子的化合物,此化合物的电子式为 。
(3)X、Y、Z三种元素组成的化合物中存在的化学键类型为 。
(4)Z、W两种元素的最高价氧化物对应水化物溶液之间反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是向100mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( ) 
A.原来盐酸的物质的量浓度为0.1molL﹣1
B.可以选择红色石蕊作为指示剂
C.氢氧化钠的物质的量浓度为0.1molL﹣1
D.pH为7时加入的氢氧化钠的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰酸锂(LiMn2O4)可作为锂离子电池的正极材料.工业上利用软锰矿浆吸收含硫烟气(SO2 和O2)制备锰酸锂,生产流程如图1: 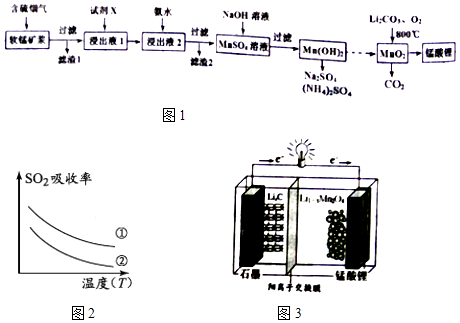
已知:①软锰矿主要成分为MnO2 , 含少量Fe2O3、FeO、Al2O3、SiO2等杂质.
②软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强.
③部分氢氧化物沉淀相关的溶液pH如表一:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
(1)已知:(图2)表二 表二
实验序号 | SO2浓度(gm﹣3) | 烟气流速(mLmin﹣1) |
① | 4.1 | 55 |
② | 4.1 | 96 |
下列措施可提高SO2吸收率的是(填序号)
a.降低通入含硫烟气的温度 b.升高通入含硫烟气的温度
c.减少软锰矿浆的进入量 d.减小通入含硫烟气的流速
(2)加入试剂X能提高产品纯度,则X可以是(填化学式)
(3)加氨水调溶液pH在5~6之间,目的是 .
(4)锰酸锂可充电电池(图3)的总反应式为:Li1﹣xMnO4+LixC ![]() LiMnO4+C(x<1) ①放电时,电池的正极反应式为
LiMnO4+C(x<1) ①放电时,电池的正极反应式为
②充电时,若转移1mole﹣ , 则石墨电极将增重g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到预期目的是( )
A. 用酒精萃取碘水中的碘
B. 用分液法分离花生油和水
C. 海盐经过溶解、过滤、蒸发制纯净的NaCl
D. 将气体通过灼热CuO以除去O2中混有的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ni2O3主要用作陶瓷、搪瓷和玻璃的着色剂,也可用于镍粉的制造.以镍粉废料为原料制备Ni2O3的工艺如图1 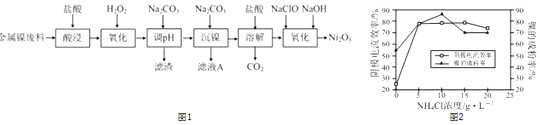
回答下列问题:
(1)Ni2O3中Ni的化合价为 .
(2)提高“酸浸”、“酸溶”速率时,温度不宜过高,其原因是 .
(3)加入H2O2“氧化”的离子方程式为;滤渣A的主要成分是(填化学式).
(4)工艺中分步加入Na2CO3的作用是;为提高原料的利用率,应控制加入NaClO与NaOH的物质的量之比为 .
(5)工业上,用镍为阳极,电解0.1mol/L NiCl2溶液与一定量NH4Cl组成的混合溶液,可得高纯度的球形超细镍粉.当其他条件一定时,NH4Cl的浓度对阴极电流效率(电流效率是指电解时,在电极上实际沉积的物质的量与理论析出量之比)及镍的成粉率的影响如图2所示: ①为获得高纯度的球形超细镍粉,NH4Cl溶液的浓度最好控制为mol/L.
②当NH4Cl溶液的浓度大于15g/L时,阴极有气体生成,导致阴极电流效率降低,请结合平衡移动原理解释其原因: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关纸层析法实验的说法正确的是( )
A.滤纸作为固定相,滤纸上吸附的水作为流动相
B.滤纸作为惰性支持物,滤纸上吸附的水作为流动相
C.滤纸上吸附的水作为固定相,溶于水的有机溶剂作为流动相
D.滤纸上吸附的水作为流动相,不溶于水的有机溶剂作为固定相
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com