
【题目】沙丁胺醇是一种新型药物,常用于缓解哮喘等肺部疾病,其一种合成路线如图:
已知:RX+![]() →
→![]() +HX
+HX
请回答:
(1)化合物C的结构简式为___。
(2)反应⑦的化学方程式为___。
(3)下列说法不正确的是___。
A.化合物A能与FeCl3溶液发生显色反应
B.化合物B能发生消去反应
C.1 mol 化合物D最多能与3mol NaOH反应
D.沙丁胺醇的分子式为C13H19NO3
(4)写出同时符合下列条件的化合物E的所有同分异构体的结构简式___。
①IR谱表明分子中含有﹣NH2,且与苯环直接相连;
②1H﹣NMR谱显示分子中有五种不同化学环境的氢原子,且苯环上只有一种氢原子。
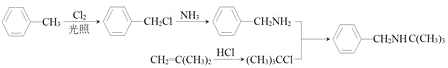
(5)请设计以甲苯和异丁烯[CH2=C(CH3)2]为原料合成化合物E的合成路线___(用流程图表示,无机试剂任选)。
【答案】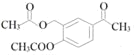
 +2H2O
+2H2O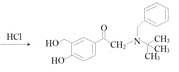 +2CH3COOH BC
+2CH3COOH BC  、
、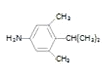 、
、 、
、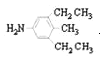
 或
或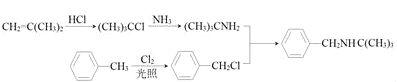
【解析】
结合沙丁胺醇( )及合成流程可知,
)及合成流程可知,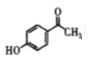 与HCHO发生加成反应生成A为
与HCHO发生加成反应生成A为 ,A与HCl发生取代反应生成B为
,A与HCl发生取代反应生成B为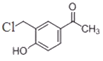 ,③为B与醋酸钠的取代反应,结合
,③为B与醋酸钠的取代反应,结合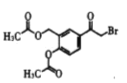 可知,④⑤均为取代反应,C为
可知,④⑤均为取代反应,C为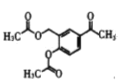 ,
, 与
与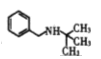 发生取代反应生成F为
发生取代反应生成F为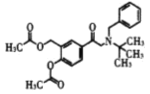 ,F与HCl发生取代反应,再发生取代反应生成沙丁胺醇;
,F与HCl发生取代反应,再发生取代反应生成沙丁胺醇;
(5)甲苯和氯气在光照条件下发生取代反应生成一氯甲苯,一氯甲苯和氨气发生取代反应生成苯胺,2-甲基丙烷和HCl发生取代反应生成(CH3)3CCl,苯胺和(CH3)3CCl发生取代反应生成E;
或2-甲基丙烷和HCl发生取代反应生成(CH3)3CCl,(CH3)3CCl和苯胺反应生成(CH3)3CNH2,甲苯发生取代反应生成一氯甲苯,一氯甲苯和(CH3)3CNH2发生取代反应生成E。
(1)通过以上分析知,C的结构简式为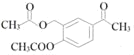 ;
;
(2)反应⑦的方程式为 +2H2O
+2H2O +2CH3COOH;
+2CH3COOH;
(3)A.A为 ,A中含有酚羟基,则化合物A能与FeCl3溶液发生显色反应,故正确;
,A中含有酚羟基,则化合物A能与FeCl3溶液发生显色反应,故正确;
B.B为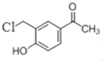 ,B中氯原子不能发生消去反应,则化合物B不能发生消去反应,故错误;
,B中氯原子不能发生消去反应,则化合物B不能发生消去反应,故错误;
C.D中水解生成的羧基、酚羟基和HBr能和NaOH反应,则1 mol 化合物D最多能与4mol NaOH反应,故错误;
D.沙丁胺醇的分子式为C13H19NO3,故正确;
故选BC;
(4)E的同分异构体符合下列条件:
①IR谱表明分子中含有﹣NH2,且与苯环直接相连;
②1H﹣NMR谱显示分子中有五种不同化学环境的氢原子,且苯环上只有一种氢原子,
则符合条件的同分异构体有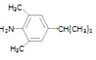 、
、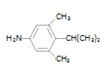 、
、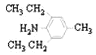 、
、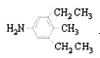 ;
;
(5)甲苯和氯气在光照条件下发生取代反应生成一氯甲苯,一氯甲苯和氨气发生取代反应生成苯胺,2﹣甲基丙烷和HCl发生取代反应生成(CH3)3CCl,苯胺和(CH3)3CCl发生取代反应生成E;或2﹣甲基丙烷和HCl发生取代反应生成(CH3)3CCl,(CH3)3CCl和苯胺反应生成(CH3)3CNH2,甲苯发生取代反应生成一氯甲苯,一氯甲苯和(CH3)3CNH2发生取代反应生成E,合成路线为:
 或
或 。
。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】如图所示,甲和乙均是双液原电池装置,下列说法不正确的是( )
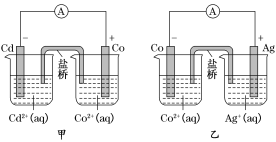
A. 甲中电池总反应的离子方程式为Cd(s)+Co2+(aq)=Co(s)+Cd2+(aq)
B. 盐桥的作用是形成闭合回路,并使两边溶液保持电中性
C. 反应2Ag(s)+Cd2+(aq)=Cd(s)+2Ag+(aq)能够发生
D. 乙电池中有1mol电子通过外电路时,正极有1mol Ag析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐中常含有少量K+、Ca2+、Mg2+、![]() 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液
(1)欲依次除去溶液Ⅰ中的Mg2+、![]() 、Ca2+,选出a所代表的试剂,按滴加顺序依次为_______溶液、_________溶液、_________溶液。(填化学式)。
、Ca2+,选出a所代表的试剂,按滴加顺序依次为_______溶液、_________溶液、_________溶液。(填化学式)。
(2)分离操作①中所用到的玻璃仪器除了玻璃棒,烧杯,还需要__________________。
(3)加盐酸的作用__________________
(4)实验室里将粗盐制成精盐的过程中,在溶解的操作中要用到玻璃棒,其作用为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸钠—过氧化氢加合物(xNa2SO4·yH2O2·zH2O)的组成可通过下列实验测定:
①准确称取1.7700g样品,配制成100.00mL溶液A。
②准确量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.5825g。
③准确量取25.00mL溶液A,加适量稀硫酸酸化后,用0.02000mol·L—1KMnO4溶液至终点,消耗KMnO4溶液25.00mL。H2O2与KMnO4反应的离子方程式如下:
2MnO4— + 5H2O2 + 6H+ =2Mn2+ + 8H2O +5O2↑。
通过计算确定样品的组成(写出必要的计算过程)。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法和解释错误的是
A. 冰融化时,需破坏晶体中的全部氢键,所以冰融化时密度变大
B. 卤化物![]() 从F到I,由于分子量增大,分子间范德华力增大,熔沸点也逐渐升高
从F到I,由于分子量增大,分子间范德华力增大,熔沸点也逐渐升高
C. 由于石墨晶体中层间距较远,电子不易实现迁移,所以石墨的导电性只能沿石墨平面的方向
D. 金属中的“电子气”在电场中可以定向移动,所以金属具有良好的导电性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 A 与 H2、CO 以物质的量 1∶1∶1 的比例形成 B,B能发生银镜反应,C 分子中只有一种氢,相关物质转化关系如下(含有相同官能团的有机物通常具有相似的化学性质):

请回答:
(1)有机物 C 的结构简式是________,反应②的反应类型是________。
(2)写出一定条件下发生反应①的化学方程式___________。
(3)下列说法不正确的是________(填字母)。
A.化合物 A 属于烃
B.化合物 D 含有两种官能团
C.用金属钠无法鉴别化合物 F、G
D.A 与 D 一定条件下可以生成 CH3CH2OCH2CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取Fe(OH)3胶体的方法是把______逐滴加在_______中,继续煮沸,待溶液呈____ 色时停止加热,其反应的离子方程式为_______________,用 __________(方法)可证明胶体已经制成,用_____方法精制胶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。预计在未来20年里,不可能有替代钕铁硼磁铁的磁性材料岀现。生产钕铁硼磁铁的主要原材料有稀土金属钕、纯铁、铝、硼以及其他稀土原料。
(1) 钕(Nd)为60号元素,在周期表中第______周期;基态铁原子的外围电子排布式为______
(2) 实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示。
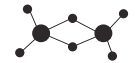
① 已知Al2Cl6分子中正负电荷中心重合,则Al2Cl6属于_________分子(填“极性”或“非极性”),分子中A1原采取______杂化。
② Al2Cl6与过量NaOH溶液反应生成Na[Al(OH)4],[A1(OH)4]-中存在的化学键有_____ (填选项字母)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(3) B元素及与其同周期相邻的两种元素第一电离能由小到大的顺序为______(用元素符号表示)。B元素可在一定条件下生成H3O+ [B(OH)F3]- ,该化合物中电负性最大的元素的原子中,所有能层电子的电子云轮廓图形状有______种
(4) 因材料中含有大量的钕和铁,容易锈蚀是它的一大弱点。可电镀镍(Ni)、锌(Zn)等进行表面涂层处理。已知Ni可以形成[Ni(NH3)6]Cl2,该配合物中配体分子的空间构型为 _______ 。
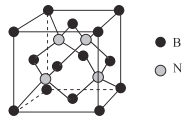
(5) 已知立方BN晶体硬而脆,其晶胞结构如图所示,设晶胞中最近的B、N原子之间的距离为anm,晶体的密度为bg·cm-3,则阿伏加德罗常数为_________ mol-1(用含a、b的代数式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com