
| A. | 加100mL水将溶液稀释 | |
| B. | 向溶液中加入0.2molNaOH固体,并使之完全溶解 | |
| C. | 将溶剂蒸发掉一半 | |
| D. | 将原溶液浓缩至50mL(无NaOH析出) |
科目:高中化学 来源: 题型:解答题
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):查看答案和解析>>
科目:高中化学 来源: 题型:填空题
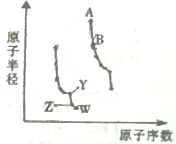 如图是元素周期表中几种短周期主族元素原子半径随原子序数的变化.
如图是元素周期表中几种短周期主族元素原子半径随原子序数的变化. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氨水吸收过量SO2气体:2NH3•H2O+SO2═2NH4++SO32-+H2O | |
| B. | FeI2溶液中通入C12至Fe2+恰好完全被氧化:2Fe2++C12═2Fe3++2C1- | |
| C. | NH4HCO3溶液与过量的NaOH溶液共热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 将1 mol•L-1 NaAlO2溶液和1.5 mol•L-1的HCl溶液等体积互相均匀混合:6AlO2-+9H++3H2O═5Al(OH)3↓+Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 LiOH是制备锂离子电池的材料,可由电解法制备.工业上利用如图装置电解制备 LiOH,两电极区电解 液分别为LiOH和LiCl溶液( )
LiOH是制备锂离子电池的材料,可由电解法制备.工业上利用如图装置电解制备 LiOH,两电极区电解 液分别为LiOH和LiCl溶液( )| A. | B极区电解液为LiOH溶液 | |
| B. | 电极每产生22.4L气体,电路中转移2mole- | |
| C. | 电解过程中Li+迁移入B电极区、OH-迁移入A电极区 | |
| D. | 电解池中总反应方程式为:2HCl$\frac{\underline{\;通电\;}}{\;}$2H2↑+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
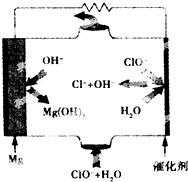 镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运及污染小等特点.如图为镁--次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是( )
镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运及污染小等特点.如图为镁--次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是( )| A. | 该燃料电池中镁为负极,发生氧化反应 | |
| B. | 正极反应式为ClO-+H2O+2e-═Cl-+2OH- | |
| C. | 电池总反应式为Mg+ClO-+H2O═Mg(OH)2↓+Cl- | |
| D. | 放电过程中OH-移向正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AB2 | B. | BA2 | C. | AB | D. | A2B2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、NO2、CO2均属于大气污染物 | |
| B. | 酸雨是pH小于5.6的降水 | |
| C. | CO2也会导致酸雨的形戒 | |
| D. | 大气中O2含量的增加会导致温室效应加剧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 g 98%的浓硫酸中含氧原予总数为4NA | |
| B. | 常温常压下,18g重水(D2O)中所含的电子数为10 NA | |
| C. | 常温常压下,4.6 g NO2气体含有0.3 NA个原子 | |
| D. | 常温下,2.7g、铝片投入足量的浓硫酸中,产生的SO2,分子数为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com