
| O | 2- 7 |
| 1.2g |
| 120g/mol |
| 1.2g |
| 120g/mol |
| 0.0015mol | ||
|


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案科目:高中化学 来源: 题型:
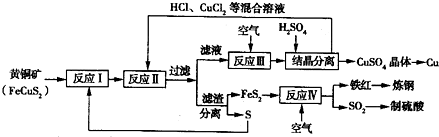
 如图所示是一种新近开发的固体氧化物燃料电池.它以掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体为固体电解质,在熔融状态下传导氧离子(O2-),其中多孔电极a、b均不参与电极反应.下列判断不正确的是( )
如图所示是一种新近开发的固体氧化物燃料电池.它以掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体为固体电解质,在熔融状态下传导氧离子(O2-),其中多孔电极a、b均不参与电极反应.下列判断不正确的是( )查看答案和解析>>
科目:高中化学 来源:2010年广东省中山市高二上学期期中考试化学卷 题型:选择题
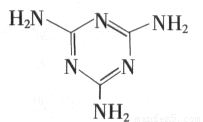
三聚氰胺(结构式如图所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域。一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量。下列说法正确的是
 A.三聚氰胺是一种蛋白质
A.三聚氰胺是一种蛋白质
B.三聚氰胺是高分子化合物
 C.三聚氰胺分子中含有碳碳双键
C.三聚氰胺分子中含有碳碳双键
D.三聚氰胺的分子式为C3H6N6
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
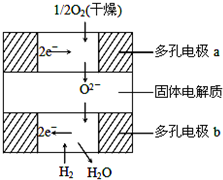
| A.采用多孔电极的目的是易于吸附气体 |
| B.有H2放电的b极为电池的负极 |
| C.a极对应的电极反应为O2+2H2O+4e-=4OH- |
| D.b极对应的电极反应为2H2-4e-+2O2-=2H2O |
查看答案和解析>>
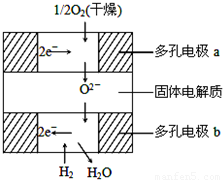
科目:高中化学 来源:2012-2013学年湖北省武汉市四校联考高三(上)月考化学试卷(10月份)(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com