
下列离子方程式正确的是
A.1mol Cl2通入含有2mol FeI2的溶液中:2Fe2++2I﹣+2Cl2=2Fe3++4Cl﹣+I2
B.澄清石灰水与少量小苏打溶液混合:Ca2++OH﹣+HCO3﹣=CaCO3↓+H2O
C. AlCl3溶液中加入过量氨水:Al3++4OH﹣=AlO2﹣+2H2O
D.向银氨溶液中加入足量的盐酸:[Ag(NH3)2]++OH﹣+3H+=Ag++2NH4++H2O
科目:高中化学 来源:2013-2014重庆市下学期期中考试高一化学试卷(解析版) 题型:选择题
下列顺序正确的是( )
A.熔点: SiO2 < NaF<KCl B.水溶性:NH3<SO2<HCl
C.酸性:HF>HCl>HI D.碱性:Mg(OH)2<KOH<RbOH
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市六校高三5月第三次诊断性考试理综化学试卷(解析版) 题型:填空题
(14分)药物菲那西汀的一种合成路线如下:

(1)菲那西汀的分子式
(2)反应①②④⑤中在苯环上发生取代反应的是
(3)反应②中生成的无机物是水和 (填化学式)
(4)写出反应⑤的化学方程式________________________________________________
(5)菲那西汀在硫酸催化下水解的化学方程式是_____________。
(6)菲那西汀的同分异构体中,符合下列条件的共有 种。
①含苯环且只有对位两个取代基 ②苯环上含有氨基 ③能水解,水解产物能发生银镜反应。
(7)菲那西汀的同分异构体中,含苯环且只有对位两个取代基,两个取代基含有相同碳原子数,且含有α-氨基酸结构,写出这种同分异构体缩聚后高分子产物的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市主城七区高三下学期第二次联考理综化学试卷(解析版) 题型:选择题
下述实验方案能达到实验目的的是
选项 | A | B | C | D |
实验 方案 |
食盐水 | 片刻后在Fe电极附近 滴入K3[Fe(CN)6]溶液 |
酸性KMnO4溶液 |
置于光亮处 |
实验 目的 | 验证铁钉发生了 析氢腐蚀 | 验证Fe电极被保护 | 验证乙烯的产生 | 验证甲烷与氯气发生了化学反应 |
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期高三第二次诊断测试理科综合化学试卷(解析版) 题型:填空题
(15分)铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)单质铁属于______晶体,将FeCl3溶液加热蒸干,灼烧所得的物质是______ (填化学式):
(2)请写出铝与氢氧化钠溶液反应的化学方程式______________________________
(3)金属Cu单独与氨水或单独与双氧水都不反应,但可与二者的混合溶液反应生成深蓝色溶液,在该深蓝色的浓溶液中加入乙醇所产生的现象是______,画出呈深蓝色的离子的结构式______.
写出Cu与氨水、双氧水反应的离子方程式:____________________________________.
(4)在硫酸亚铁溶液中加入过量的碳酸氢铵,有FeCO3沉淀生成,写出其化学方程式____________.
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市万州区高三考前模拟理综化学化学试卷(解析版) 题型:实验题
(15分)
某化学兴趣小组利用以下各装置连接成一整套装置,探究氯气与氨气之间的反应.其中D为纯净干燥的氯气与纯净干燥氨气反应的装置.

请回答下列问题:
(1)连接好装置后,必需进行的一步实验操作是 。
(2)装置E的作用是 ,橡胶管k的作用是 。
(3)从装置D的G处逸出的尾气中可能含有黄绿色的有毒气体,处理方法是 。
(4)装置F中试管内发生反应的化学方程式____ 。
(5)接入D装置的两根导管左边较长、右边较短,目的是______ .
(6)整套装置从左向右的连接顺序是(j)接( )( )接(f)(g)接( )( )接( )( )接(a).
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市万州区高三考前模拟理综化学化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是
A.在反应中消耗1mol Cl2,转移的电子数一定为2NA
B.标准状况下,0.5mol氦气含有的电子数为NA
C.15gCH3+(碳正离子)中含有电子数为10NA
D.0.1L 2 mol·L-1的(NH4)2S溶液中含有的S2-数目为0.2NA
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:填空题
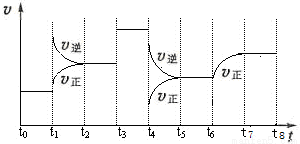
(12 分)T℃时,在某容积恒为2L密闭容器中充入2molN2、4molH2,在催化剂辅助下发生反应:N2(g)+3H2(g) 2NH3(g) △H=-92.0kJ /mol。t0时刻,建立平衡后,测得生成NH3的量为2mol;从t1时刻开始,改变反应的一个条件,体系中反应速率随时间变化的情况,如下图所示。
2NH3(g) △H=-92.0kJ /mol。t0时刻,建立平衡后,测得生成NH3的量为2mol;从t1时刻开始,改变反应的一个条件,体系中反应速率随时间变化的情况,如下图所示。
试回答下列问题:
(1)T℃时,N2的转化率为:___________,该反应的平衡常数K=___________。
(2)T℃时,下列能证明该反应已经建立平衡状态的是:__________________。
A.体系总压强不再改变
B.混合气体颜色不再改变
C.H2的质量百分含量不再改变
D.c(N2)与c(NH3)的比值不再改变
(3)t1时刻,改变的外界条件是__________,平衡常数K(t5~t6) ______ K(t7~t8)(填“>、<或=”,下同)。
(4)T℃时,建立平衡后,向容器中加入2molN2和2molNH3,则此时 v正 ___ v逆。
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省大连市高三双基测试化学试卷(解析版) 题型:选择题
在分子式为C4H10O的有机物中,含有—OH的同分异构体有(不考虑立体异构)
A.5种 B.4种 C.3种 D.2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com