
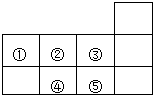
| A. | 元素①位于第二周期第ⅣA族 | B. | 气态氢化物的稳定性:④>② | ||
| C. | 元素的最高正化合价:③=⑤ | D. | 最高价氧化物对应水化物酸性:⑤>④ |
分析 A.由元素在周期表中的位置可知,元素①位于第二周期第ⅤA族;
B.同主族自上而下非金属性减弱,非金属性越强氢化物越稳定;
C.由元素在周期表中的位置可知,③为F,⑤为Cl,氟元素没有正化合价;
D.同周期自左而右,非金属性增强,非金属性越强最高价氧化物对应水化物的酸性.
解答 解:A.由元素在周期表中的位置可知,元素①位于第二周期第ⅤA族,故A错误;
B.同主族自上而下非金属性减弱,非金属性越强氢化物越稳定,故气态氢化物的稳定性:④<②,故B错误;
C.由元素在周期表中的位置可知,③为F,⑤为Cl,Cl元素最高正化合价为+7,而氟元素没有正化合价,故C错误;
D.同周期自左而右,非金属性增强,非金属性越强最高价氧化物对应水化物的酸性,故酸性:⑤>④,故D正确;
故选D.
点评 本题考查元素周期表与元素周期律的关系,题目难度中等,注意掌握元素周期律内容、元素周期表结构,明确O、F元素没有正化合价及一些元素的特殊性.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,D原子的原子结构示意图为
,D原子的原子结构示意图为 ,C+离子的结构示意图为
,C+离子的结构示意图为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某水溶液中加入氯化钡溶液发现有白色沉淀生成即可证明该溶液中含有硫酸根离子 | |
| B. | 某盐溶液加入盐酸产生二氧化碳,该盐一定为碳酸盐 | |
| C. | 将O2和H2的混合气体通过灼热的CuO,以除去其中的H2 | |
| D. | 加稀盐酸后过滤,以除去混在铜粉中的少量镁粉和铝粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 配料表 | 精制海盐、碘酸钾 |
| 含碘量 | 20~40mg/kg |
| 卫生许可证号 | ××卫碘字(1999)第001号 |
| 分装日期 | 见封底 |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com